|
|
|
Структурирование сублиторальной растительности дальневосточных морей России с точки зрения концепции адаптивной зоны
Дуленин А.А. Alexander A. Dulenin
Хабаровский филиал ГНЦ РФ ФГБНУ «Всероссийский научно-исследовательский институт
УДК 574.58
Предложена экологически обоснованная методология выделения, описания, инвентаризации и оценки ресурсов сообществ морской сублиторальной растительности. Установлено, что пояс сублиторальной растительности дальневосточных морей России сформирован системой адаптивных зон разного ранга. Распределение растительности в отдельных районах обусловлено географией и геоморфологией их берегов. Любые описания растительных сообществ принципиально сравнимы при условии выделения главного доминанта, для которого на участке формируется адаптивная зона. В регионе выделено 67 растительных ассоциаций, большинство из которых может быть однозначно опознано визуально. Число ассоциаций уменьшается от южных районов к северным. Характер их распределения следует описывать как ценотический аспект закона Гумбольдта-Уоллеса. Ресурсы отдельных видов приурочены к их адаптивным зонам, площадь промысловых поселений равна площади зон. Объем ресурсов макрофитов Дальнего Востока оценен в 3,6 млн т. Ключевые слова: структура растительности; сублитораль; Дальневосточные моря России
Введение Настоящее сообщение представляет собой краткий обзор опыта автора по структурированию дальневосточной сублиторальной растительности, более полно изложенного в его докторской диссертации (Дуленин, 2024а). Необходимость в такой работе возникла в связи с тем, что Дальний Восток России – регион со слабо изученной сублиторальной растительностью. Ее сообщества описывали преимущественно на локальных участках Приморья (Скарлато и др., 1967; Калита, Скрипцова, 2014), на Курилах (Гусарова, 1975; Евсеева, 2007) и у берегов Сахалина (Голиков и др., 1985; Петров, Поздеев, 1992). Ряд публикаций имеют описательный характер и почти не содержат количественных характеристик растительности (Блинова, 1971; Перестенко, 1980, 1997). Обобщающие работы не имеют сведений о ценотической структуре растительного покрова (Гусарова и др., 1993) или носят компилятивный характер (Суховеева, Подкорытова, 2006; Блинова, 2014; Ресурсы …, 2020). Систематические обобщения, в которых содержались бы единообразные ценологические характеристики сублиторальной морской дальневосточной растительности, до сих пор отсутствуют. Проблемой является принципиальная возможность приведения к «общему знаменателю» разнородных количественных и качественных описаний растительности, поскольку методические и методологические подходы к ее описанию разнятся, а данные, полученные разными исследователями, нередко представляются несопоставимыми (Афанасьев, Рубан, 2013; Дуленин, 2023). Общая синтаксономическая классификация сублиторальной растительности дальневосточных морей России до сих пор не было разработана. Развитие науки о растительности традиционно было связано с решением практических задач, таких как рациональное использование растительных ресурсов (Шенников, 1964; Быков, 1978). Однако имеющиеся работы, посвященные морской растительности региона, не имеют практической направленности: обычно с их помощью нельзя оценить ресурсы макрофитов, сложно получить и прочие прикладные экологические характеристики. Для исследования статистических закономерностей распределения макрофитов на инфраценотическом уровне и количественного описания ассоциаций растительности были выбраны модельные районы: южный низкобореальный у северо-западного побережья Японского моря, протяженный на 600 км с юга на север и северный высокобореальный у северо-западного побережья Охотского моря, простирающийся на 1000 км с юго-запада на северо-восток (рис. 2). Сведения о структуре их растительности с некоторыми оговорками могут быть экстраполированы на аналогичные районы Дальнего Востока. Настоящая работа преследовала цель выявить принципиальные возможности сравнения и общие характеристики сложения сублиторальной морской растительности различных районов Дальнего Востока России. Состояние изученности макрофитобентоса региона. В исследованиях макрофитобентоса дальневосточных морей выделено три основных направления.
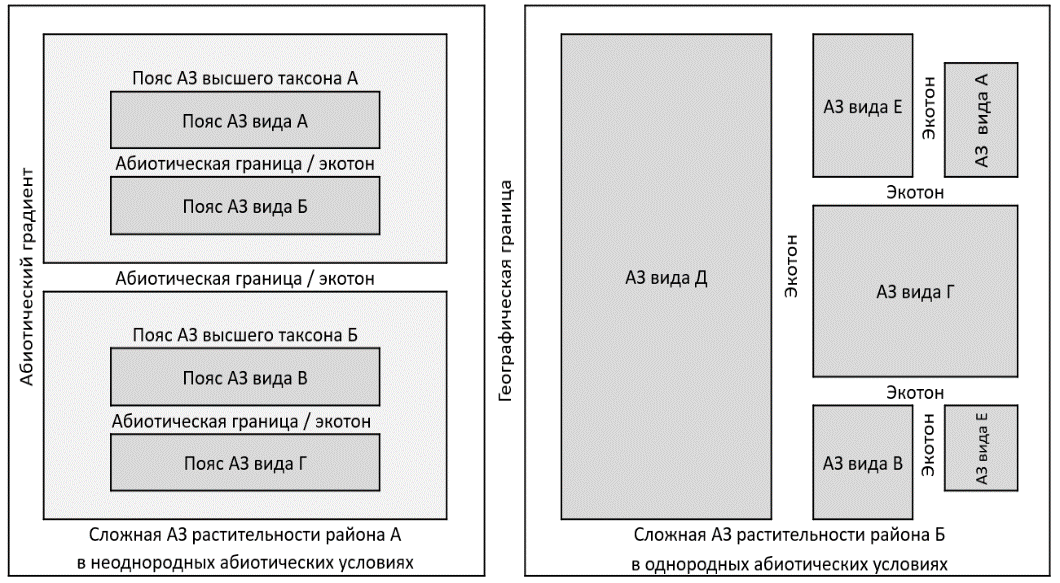
Выбор подходов для описания сублиторальной растительности Дальнего Востока России. Сказанное позволяет сформулировать основную проблему настоящей работы: до сих пор отсутствовала независимая от мнения исследователя и ценологически оправданная методологическая основа для инвентаризации донной морской растительности и ее ресурсов. Подходы к решению этой проблемы обозначены в предыдущих публикациях автора (Дуленин, 2023, 2024б). Биологически адекватное описание донной морской растительности требует наличия общей концепции, которая объясняла бы наблюдаемый характер распределения макрофитобентоса. Для морской растительности умеренных и высоких широт типично формирование поселений, в которых структура сообщества определяется единственным видом, в то время как обилие прочих оказывается существенно ниже (Скарлато и др., 1967; Огородников, 2003; Селиванова, 2004; Taniguti, 1962; den Hartog, 2016 и др.). Такая структура соответствует концепции адаптивной зоны (Симпсон, 1948; Волвенко, 2018; Volvenko, 2022). Ее формирование обусловлено комплексом адаптаций некоторых организмов к условиям среды, обеспечивающих им наибольший успех в размножении (по: Симпсон, 1948). Адаптивные зоны разделены относительно выраженными границами и преобладают в модельных районах (Дуленин, 2023, 2024б). Узкие адаптивные зоны отдельных видов слагаются в системы широких зон высших таксонов. Пояса растительности отдельных районов целесообразно рассматривать как сложные адаптивные зоны. Они должны представлять собой систему из соподчиненных ячеек, состоящих из поясов, сложенных представителями высших таксонов и отдельных видов, разделенных экотонами, приходящимися на участки смены экологических условий (рис. 1, слева), либо хаотичную мозаику адаптивных зон отдельных видов (рис. 1, справа) в однородных условиях.
Рис. 1. Схема структуры сложных адаптивных зон (АЗ)
Существует два крайних противоположных взгляда на природу биотического сообщества: по К. Мёбиусу это виды, связанные биотическими связями, а по К. Петерсену это лишь механический набор видов (Möbius, 1877; Petersen, 1913, 1918, по: Несис, 1977; Волвенко, 2018). Если сообщество опознается по единственному виду, оно является элементарным петерсеновским сообществом и эквивалентно адаптивной зоне (Волвенко, 2018). В таком случае ассоциация в условиях доминантной сублиторальной растительности – это группа фитоценозов с общим главным доминантом, расположенным на определенной площади в пространственных границах своей адаптивной зоны. Тогда соотношение используемых в работе понятий следующее: адаптивная зона отражает приспособительный аспект сообщества, элементарное петерсеновское сообщество – ценотический аспект по степени выраженности связей между видами, а ассоциация – его классификационный аспект. Системы зон, образуемые высшими таксонами, в этом случае должны в некоторой степени соответствовать и высшим синтаксонам в классификации растительности. Сами высшие синтаксоны также должны быть не классификационными абстракциями, а реальными сообществами со своим расположением в пространстве. На основании сказанного была сформулирована основная гипотеза этой работы: пояс сублиторальной растительности представляет собой систему адаптивных зон, сложенных петерсеновскими сообществами. Условия обитания сублиторальной растительности в дальневосточных морях России. Регион исследования (рис. 2) расположен у северо-восточных побережий Азиатского материка, омываемых водами Тихого океана и его морями – Японским, Охотским и Беринговым. Фитогеографически он почти полностью охватывает приазиатскую часть бореальной зоны, которая разделяется на низкобореальную и высокобореальную подзоны (Перестенко, 1994).
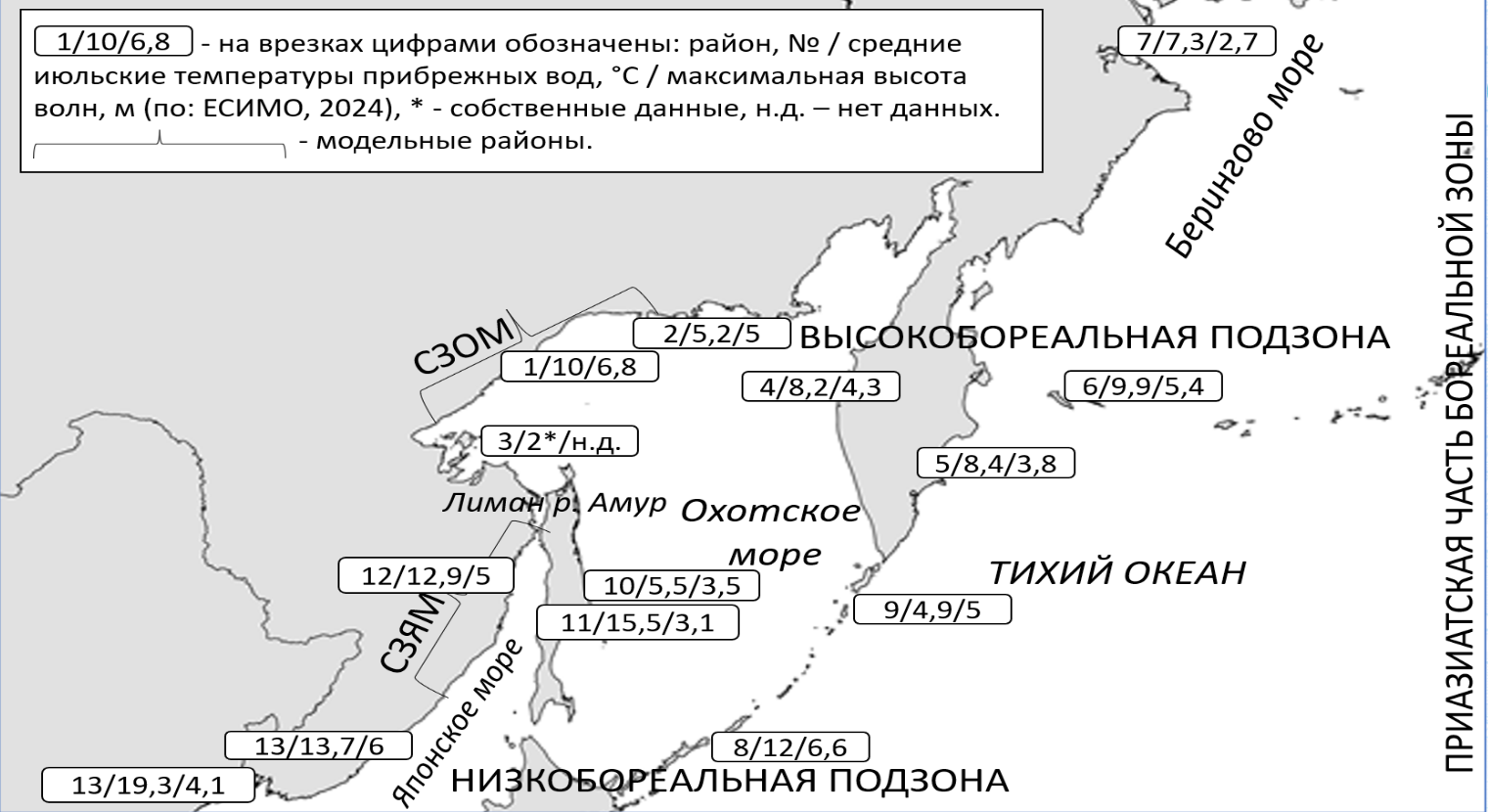
Рис. 2. Фитогеографическое зонирование (по: Перестенко, 1994), районы, температуры и высота волн прибрежных вод морей Дальнего Востока России. Районы: 1 – северо-западное побережье Охотского моря (СЗОМ), 2 – север Охотского моря, 3 – Шантарские острова, 4 – западная Камчатка, 5 – восточная Камчатка, 6 – Командорские острова, 7 – Чукотка, 8 – южные Курильские острова, 9 – северные Курильские острова, 10 – восточный Сахалин, 11 – западный Сахалин, 12 – северо-западное побережье Японского моря (СЗЯМ), 13 – Приморье
Макрофитобентос региона не испытывает недостатка в биогенах (по: Шунтов, 2001). Соленость в прибрежной зоне составляет, как правило, 30–34‰ и благоприятна для развития морской растительности. Единственной большой акваторией, где морская растительность не может существовать, является лиман р. Амур с соленостью в пределах 4,1–13,3‰ (по: ЕСИМО, 2024). Остальные абиотические условия: температура, системы течений, интенсивность волнения, геоморфологическая структура берегов – существенно различаются в разных районах и влияют на характер и распределения растительности. Рассмотрение условий ее обитания позволило сформулировать ряд гипотез в отношении растительности региона:
Сформулированные гипотезы проверены в настоящей работе.
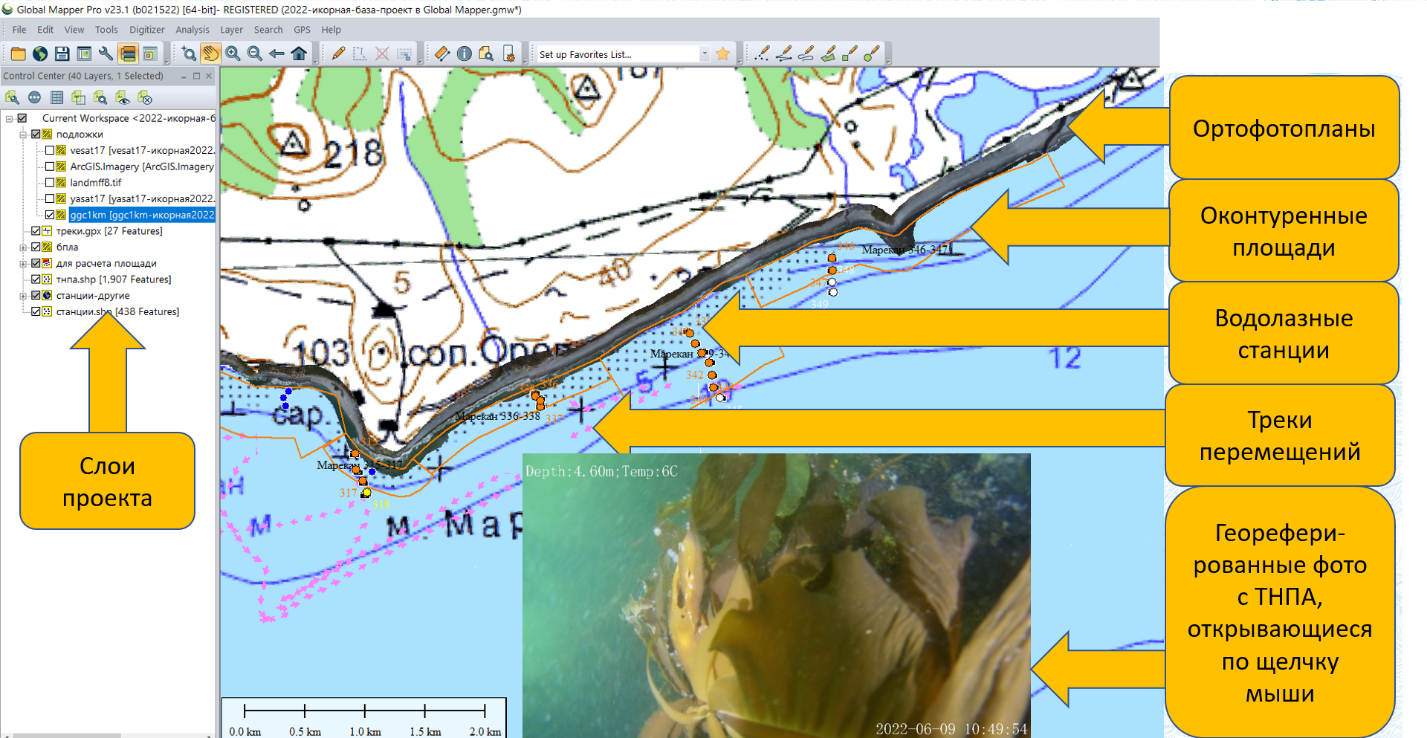
Материалы и методы Было выделено 2 модельных района: относительно тепловодный южный в северо-западной части Японского моря и холодноводный северный в северо-западной части Охотского моря – с растительностью, типичной для низкобореальной и высокобореальной подзон соответственно. Исследования проводили с 1999 по 2024 гг. в обоих модельных районах с борта среднетоннажных и маломерных судов, выполняя водолазные съемки, съемки при помощи подводных роботов и беспилотников, а также наблюдения с поверхности. В южном модельном районе выполнено 14 экспедиций (3792 гидробиологических станции), в северном – 18 экспедиций (7298 станций). Данные получены в июле–сентябре в период гидрологического лета, т.е. по летнему аспекту растительности. Регулярные водолазные съемки проводили по типическому принципу (Изучение …, 2005), на глубинах от 2 до 20 м в легководолазном снаряжении, выполняя перпендикулярные берегу гидробиологические разрезы на расстоянии 0,5–10 км друг от друга, где делали от 2 до 10 станций, в зависимости от типов побережий и однородности биоты. Удельную биомассу учитывали путем отбора проб с площадок в 0,25 м2 либо 1 м2. Проективное покрытие дна растительностью определяли глазомерно путем осмотра 10–500 м2 дна. Съемки с подводных роботов (Chasing M2 и Qysea Fifish V6) выполняли, используя выработанные методические приемы (Дуленин, Кудревский, 2019; Дуленин и др., 2022). Их применяли как инструмент рекогносцировки при водолазных съемках. Беспилотные полеты (на беспилотниках потребительского класса DJI Phantom 4 Pro v2, Mavic 2, Mini 2) выполняли по разработанным методикам (Дуленин и др., 2021) в режиме ручного управления или автоматических полетных миссий, используя программное обеспечение Map Pilot Pro, Litchi. Для обработки данных беспилотных съемок применяли программный пакет Agisoft Metashape Professional. Для ориентирования на местности использовали мобильную геоинформационную систему AlpineQuest, в которой записывали треки передвижений, координаты и характеристики станций. Атрибутивные данные съемок, подводные фотоснимки, ортофотопланы (т.е. цифровые фотомозаики местности), растровые топографические карты и космоснимки загружали в настольную геоинформационную систему Global Mapper, создавая «цифровые двойники» (Blair, 2021; Nativi et al., 2021) экосистем: многослойные интерактивные иллюстрированные карты района съемки, содержащие в виде слоев бóльшую часть ее результатов (рис. 3) и пригодные для планирования исследований, систематизации, обработки и представления данных. Их создание обеспечивало максимальную степень верифицируемости получаемых результатов.
Рис. 3. Участок выполнения комплексной съемки у северо-западного побережья Охотского моря (СЗОМ) в 2022 г. с результатами, систематизированными в геоинформационной системе Рис. 3. Участок выполнения комплексной съемки у северо-западного побережья Охотского моря (СЗОМ) в 2022 г. с результатами, систематизированными в геоинформационной системе
THE FULL-SIZED IMAGE CAN BE SEEN BY CLICKING ON THE LINK
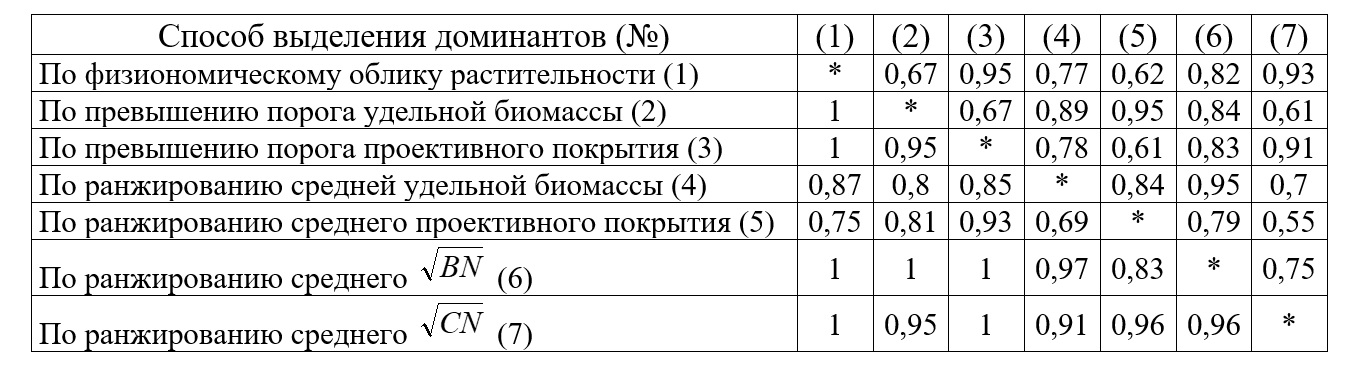
Виды идентифицировали по определителям и атласам Л.П. Перестенко (1994), Н.Г. Клочковой (1996), Н.Г. Клочковой с соавт. (2009а, б). Названия таксонов приведены по (Guiry, Guiry, 2024). В качестве промысловых учтены поселения видов в пределах своих адаптивных зон (Дуленин, 2023, 2024б). Промысловые запасы рассчитывали, суммируя произведения площади и удельных биомасс видов на промысловых участках. Оценки запасов по результатам визуальных наблюдений выполняли по разработанным методикам (Дуленин, 2016а, 2020а) на основании сопоставления оценок покрытия дна растительностью, выполняемых одновременно и независимо двумя наблюдателями. Для определения оптимальных методов выделения доминантов (Дуленин, 2020б) сравнивали их списки, полученные семью различными способами (табл. 1). Растительные ассоциации выделены на основе концепции адаптивной зоны (Волвенко, 2018; Volvenko, 2022) по описанной ранее методике (Дуленин, 2021) на принципах редукционизма (Миркин и др., 1989), обеспечивающих минимум классификационных построений, необходимых для однозначного опознания ассоциаций и высших синтаксонов. Поскольку ассоциации в большинстве случаев опознаются визуально, оценки покрытия дна растительностью считались приоритетными для их выделения (Дуленин, 2021), а оценки удельных биомасс – дополнительными. Ассоциации опознавали по главному доминанту (ГД), принадлежащему к господствующему ярусу наибольшей высоты. В качестве доминанта каждого подчиненного яруса указывали наиболее обильный в этом ярусе вид при условии достижения порогов доминирования (Баканов, 2005), принятых ранее (Дуленин, 2020б). Для того, чтобы сделать продромус растительности удобочитаемым для фитоценологов, использующих принципы Международного кодекса фитосоциологической номенклатуры (далее Кодекса), использована система флористической синтаксономии (Терийа и др., 2022). Она пригодна для синтаксономической классификации сообществ, описанных по доминантам (Василевич, 2010). Синтаксоны именовали по рекомендациям Кодекса (Терийа и др., 2022), давая латинские окончания -etum ассоциациям, -ion – союзам, -talia – порядкам, -tea – классам. Для синтаксономической классификации доминанты ассоциаций были обозначены в качестве их диагностических видов. Ассоциации с главными доминантами, принадлежащими к одному роду или семейству, объединяли в союзы растительности, с главными доминантами, принадлежащими к одному таксономическому порядку, жизненной форме или ярусу – в порядки, а принадлежащими к одному классу или отделу – в классы растительности. Первичные гидроботанические описания представляют собой данные для служебного пользования и полное их опубликование в соответствии с рекомендациями Кодекса (Терийа и др., 2022) невозможно. Поэтому таблицы с характеристиками ассоциаций содержат обобщенные статистические данные вместо первичных описаний. Для установления градиентных закономерностей изменения количественного обилия доминантов использовали процедуры регрессионного анализа. Для установления сходства между разными участками растительности использовали кластерный анализ. Количественные характеристики растительности дискретных участков сравнивали с помощью подходящих параметрических и непараметрических критериев, в зависимости от характера распределения данных и объемов выборок. Статистическую обработку материалов выполняли в свободно распространяемом статистическом пакете PAST 3 (Hammer, 2023).
Результаты и обсуждение Сравнение списков доминантов подводной растительности на примере северо-западного побережья Японского моря. Выделение доминантов растительности необходимо для выявления закономерностей ее распределения на инфраценотическом (Миркин и др., 2001) и ценотическом уровнях, а также для прикладных целей (рыбохозяйственные характеристики, оценка промысловых ресурсов и т.п.). В ряде работ приводятся сведения о доминирующих видах макрофитов дальневосточных морей (Гусарова, 1975; Перестенко, 1980, Дуленин, 2008 и др.). Отсутствие количественных критериев выделения доминантов в этих работах вызывало вопросы о возможности сравнения данных разных авторов и о принципиальной верифицируемости (Popper, 2002) их результатов. Указанные вопросы требовали своего разрешения. Для этого было выполнено сравнение результатов выделения доминантов семью различными способами (табл. 1). Наименьшее их количество получено по физиономическому облику растительности (19 видов, 12% видового состава макрофитов сублиторали), наибольшее – по превышению условного порога проективного покрытия (25 видов, 16% видового состава). Среднее количество доминантов (по 21 виду, 14%) выделено по пороговому значению удельной биомассы и ранжированию ее средних значений, а также по обоим использованным коэффициентам доминирования. Списки доминантов сходны по размеру, их длина отличается не более чем на четверть. Сходство числа доминантов следует рассматривать, как один из признаков адекватности каждого из примененных способов их выделения. Все списки при попарном сравнении статистически неразличимы (табл. 1), что также говорит о сопоставимости примененных способов. Таблица 1. Уровни статистических различий списков доминантов сублиторальной растительности северо-западной части Татарского пролива, выделенных различными способами Table 1. Levels of statistical differences in the lists of dominant species of sublittoral vegetation along the northwestern coast of the Sea of Japan, identified using different methods
Примечание. Выше диагонали – вероятность ошибочного отклонения нулевой гипотезы р по критерию Фишера, ниже – по критерию Андерсона; Note. Above the diagonal is the probability of incorrectly rejecting the null hypothesis p according to Fisher's test; below is the probability according to Anderson's test;
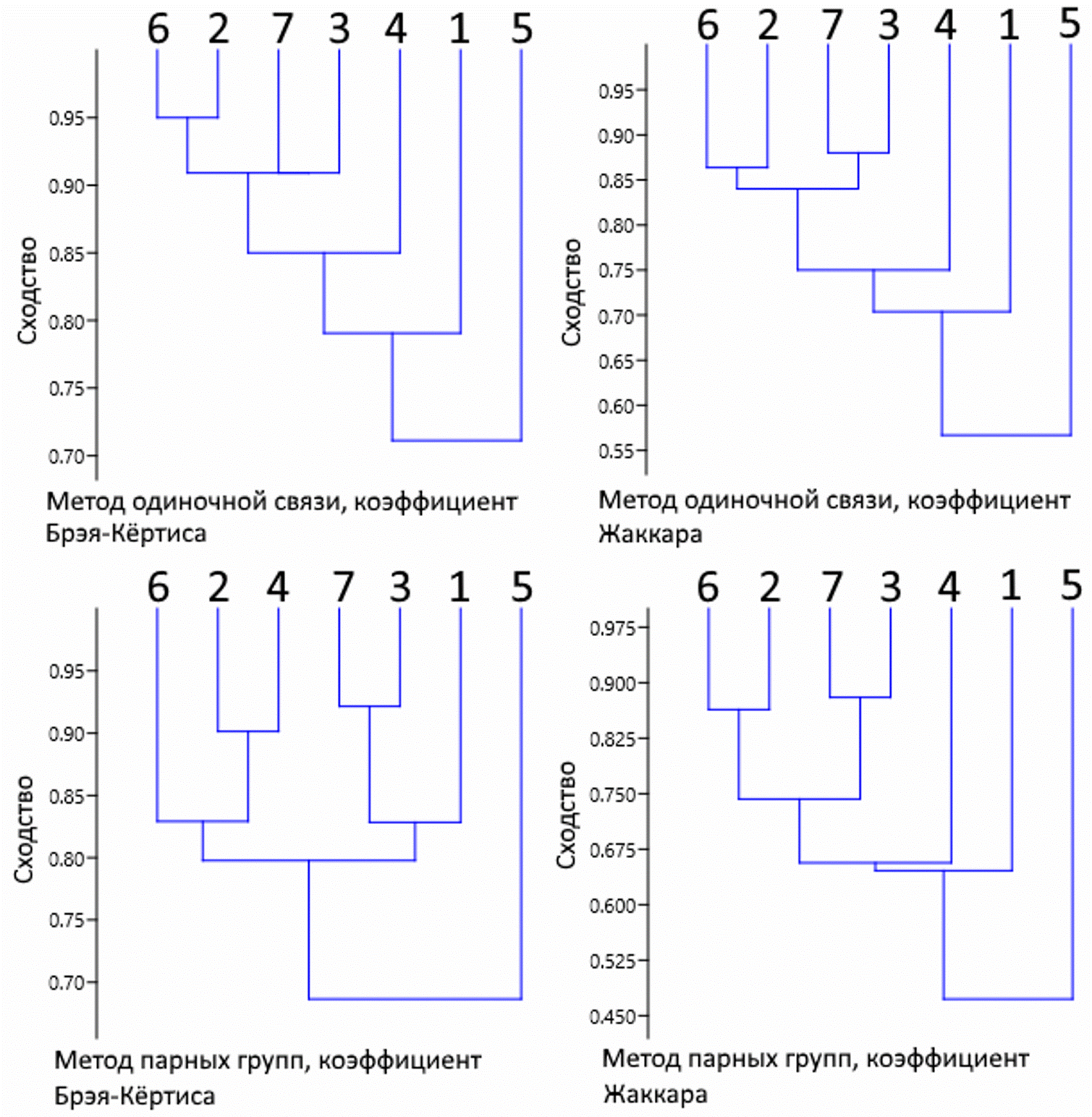
Результаты кластерного анализа (рис. 4) показали согласованную картину: уровни сходства большинства списков доминантов высоки. Таким образом, адекватность оценок доминирования верифицируется различными способами выделения доминантов, основанными как на субъективных визуальных оценках, так и на инструментальном учете обилия. Визуально определяемые величины проективного покрытия принципиально пригодны для выделения доминантов. Однако очевидно, что 7 способов выделения доминантов для практики избыточны.
Рис. 4. Уровень сходства состава доминантов сублиторальной растительности у северо-западного побережья Японского моря, выделенных различными способами. Цифровые обозначения см. в табл. 1
Действительно, 16% состава сублиторальной флоры, входящие в самый длинный список доминантов (25 видов по порогу проективного покрытия, № 3), занимают 81% площади дна и формируют 85% биомассы в пределах адаптивных зон пояса растительности южного модельного района. Остальными видами в большинстве практических исследований можно пренебречь. В то же время для прикладных изысканий недостаточно единственного показателя доминирования, т.к. для них используются величины как биомассы, так и относительной площади, занимаемой видами. Поэтому был предложен следующий общий алгоритм выбора способов оценок доминирования в зависимости от масштабов и задач исследования (Дуленин, 2020б):
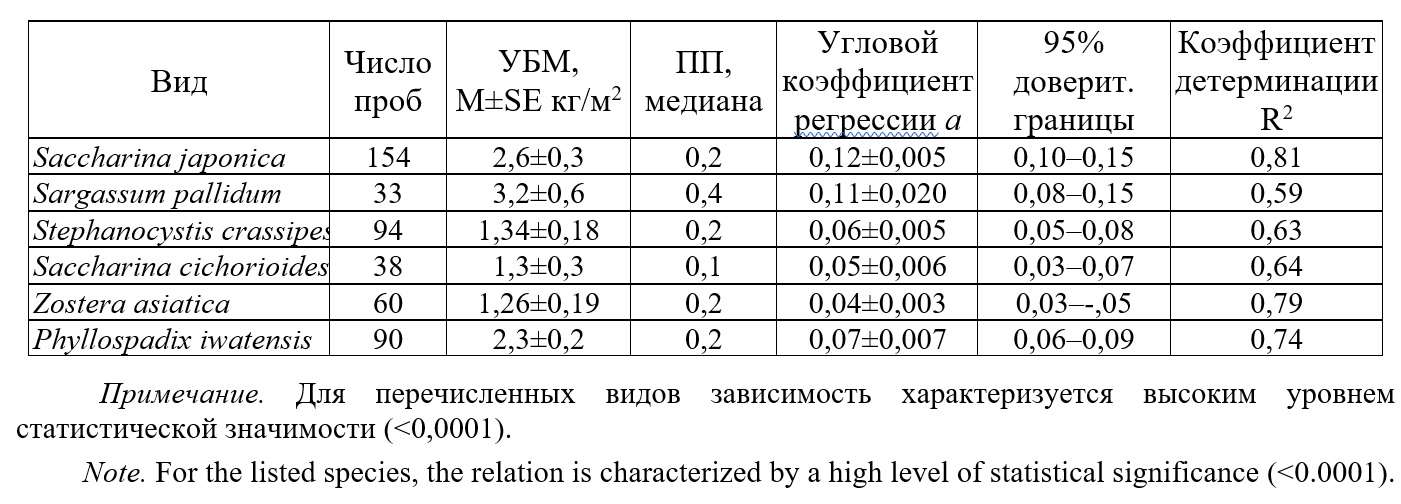
По К. Попперу (Popper, 2002), критериями, позволяющими считать исследование научным, являются принципиальная возможность проверки и опровержения его результатов. Распространены взгляды, что визуальные оценки основаны на личном мнении, которое не может быть твердым основанием для принятия управленческих решений (Madsen, Bloomfield, 1993). Поэтому в южном модельном районе были проверены возможности верификации субъективных количественных оценок. Таблица 2. Описательные статистики и показатели зависимости удельной биомассы (УБМ) и проективного покрытия (ПП) для макрофитов у северо-западного побережья Японского моря Table 2. Descriptive statistics and relation indicators between specific biomass and projective cover for macrophytes off the northwest coast of the Sea of Japan
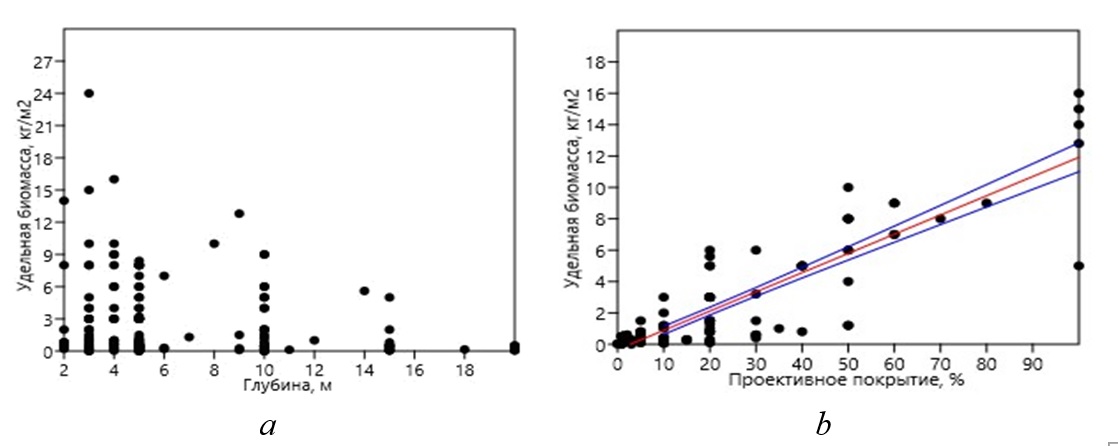
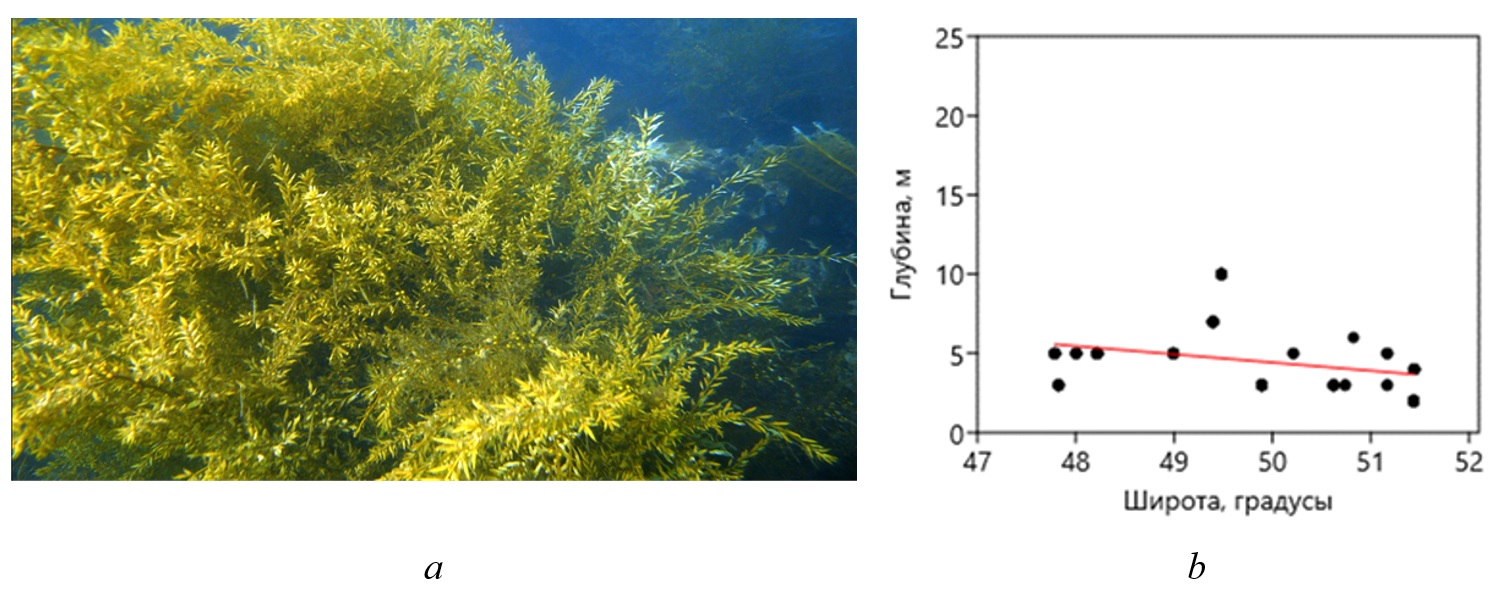
Очевидно, что практическое использование визуальных данных о проективном покрытии возможно при условии, если его можно удовлетворительно пересчитать в биомассу. Было установлено, что в южном модельном районе для промысловых видов зависимость между покрытием и удельной биомассой хорошо выражена (Дуленин, 2016а) и позволяет выполнять такие пересчеты (табл. 2). В северном модельном районе данные о покрытии оказались непригодны для пересчета в биомассу (Дуленин, 2015), поскольку их получали после нереста сельди, когда макрофиты покрыты ее икрой, которая скрадывает имеющиеся зависимости. Поселения сахарины японской – промыслового вида, определяющего облик растительности южного модельного района (рис. 5a), приурочены к доступным для визуальных наблюдений мелководьям, а связь покрытия и биомассы сильно выражена (табл. 2, рис. 5b).
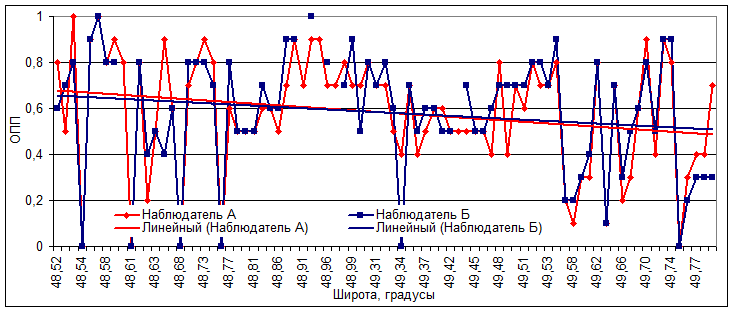
Рис. 6. Визуальные оценки покрытия дна растительностью двумя наблюдателями у северо-западного побережья Японского моря. ОПП – общее проективное покрытие
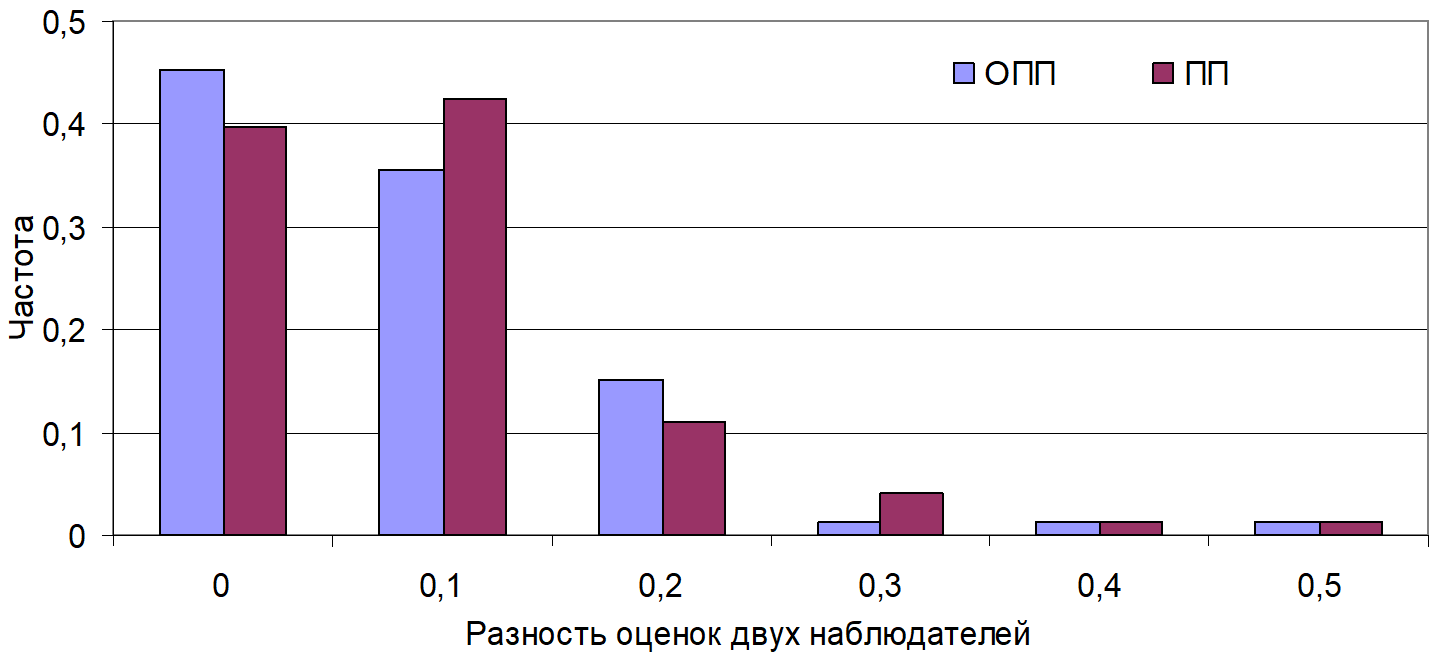
Это позволяет использовать визуальные оценки покрытия для расчета величины промысловых запасов сахарины японской. Однако отдельную задачу представляет возможность верификации субъективных визуальных наблюдений. Основной способ обеспечения верифицируемости экспертных данных при таких наблюдениях – получение согласованных независимых оценок несколькими экспертами (Рупосов, 2015). Данные независимых наблюдений оказались сходны (рис. 6): коэффициент конкордации τ оценок общего проективного покрытия дна растительностью составил 0,73, а покрытия сахарины японской – 0,78. Вероятность случайного совпадения таких наблюдений чрезвычайно мала (p<0,0001). Доли оценок с высокой степенью согласованности составили 81% для общего покрытия и 82% для покрытия сахарины японской. Плохо согласованные оценки были редки и составляли около 3% для обоих показателей (рис. 7).
Рис. 7. Распределение разностей визуальных оценок покрытия дна растительностью двумя наблюдателями у северо-западного побережья Японского моря.
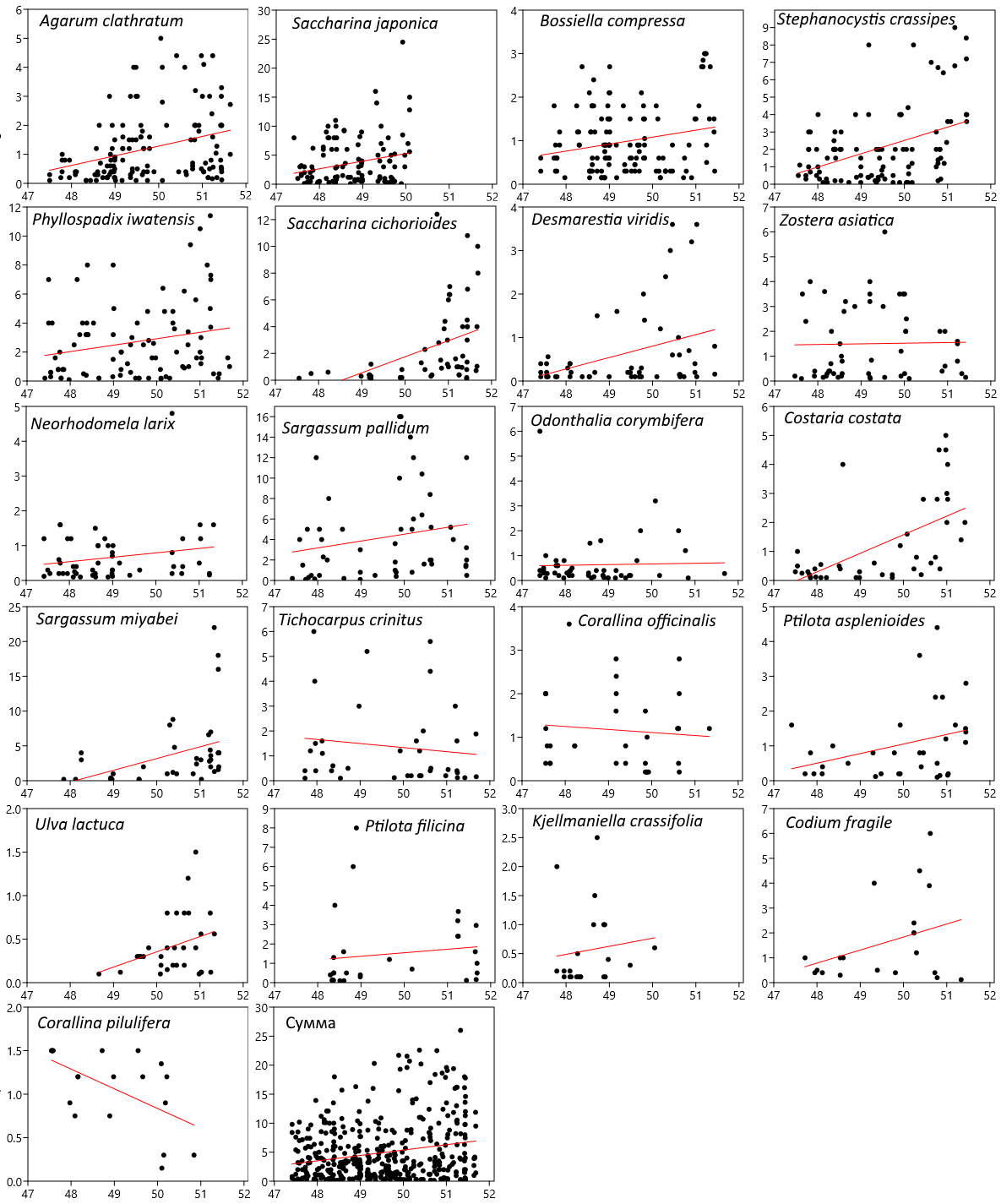
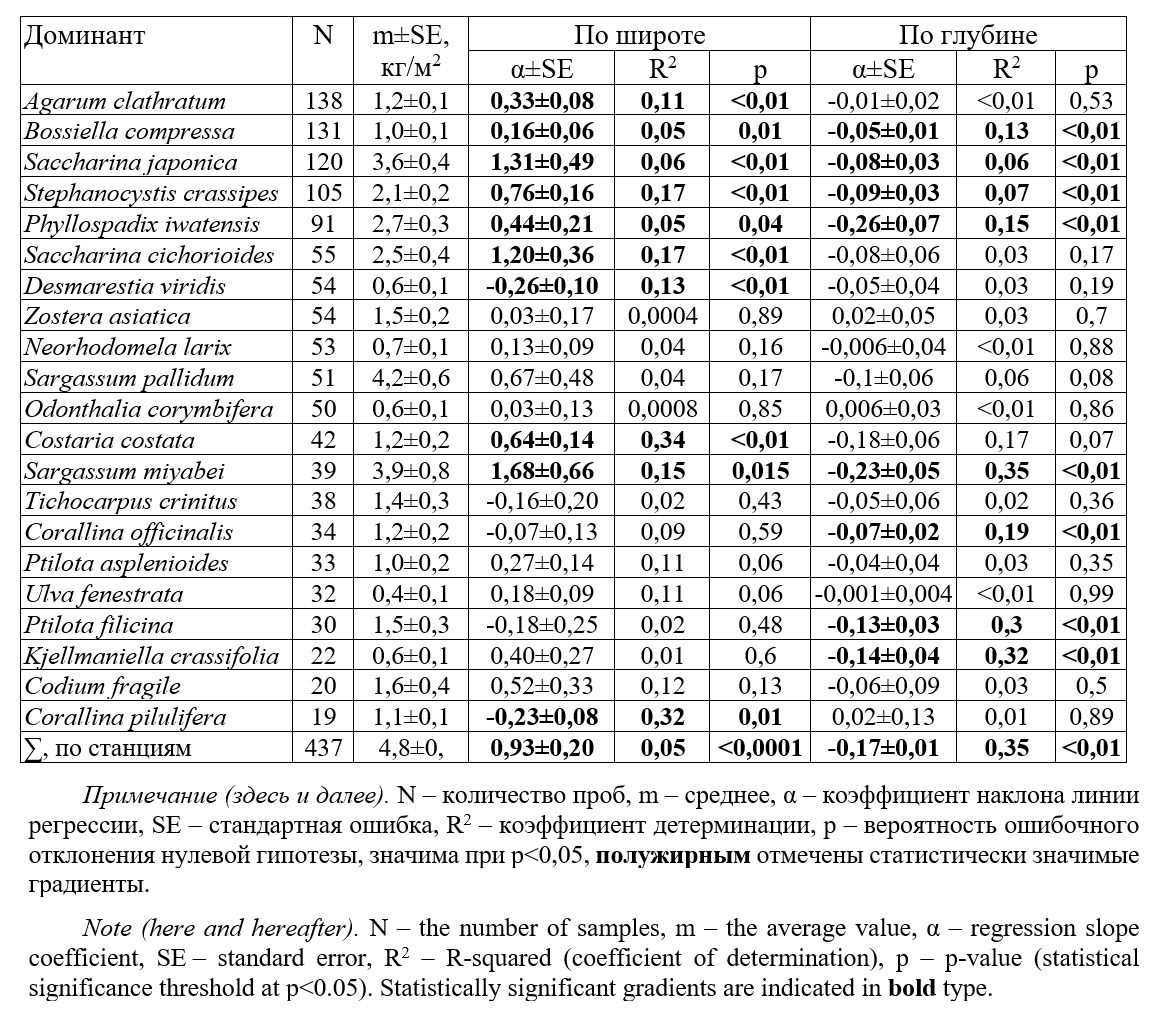
Средние значения разности в оценках общего покрытия и покрытия сахарины японской были близки (0,08±0,01 и 0,09±0,01) и статистически незначимы (p=0,55–1 для разных показателей и статистических критериев). Следовательно, оба показателя оценивались наблюдателями с сопоставимой точностью, а их наблюдения отражали объективную картину покрытия дна растительностью. Итак, применение параллельных независимых визуальных наблюдений оказалось пригодно для практического использования. Субъективные визуальные оценки проективного покрытия позволяют показывать характер и особенности пространственного распределения донной растительности и могут быть использованы для выявления и описания как общей адаптивной зоны пояса растительности, так и адаптивных зон отдельных видов. Применение визуальных наблюдений дало возможность сократить время учетных работ по оценке промыслового запаса сахарины японской на стандартном участке протяженностью 150 км в южном модельном районе на порядок (2–3 дня вместо 1 месяца), а стоимость – на 3 порядка (20–30 тыс. руб. вместо 12 млн руб. в ценах 2024 г.) по сравнению с традиционными водолазными съемками (Дуленин, 2020а). Общие закономерности пространственного распределения растительности модельных районов. Рассмотрим закономерности распределения доминантов и поясов сублиторальной растительности модельных районов как систем адаптивных зон. У северо-западного берега Японского моря на региональном инфраценотическом уровне состав и обилие доминантов меняются по широте и глубине (табл. 3, рис. 8).
Рис. 8. Распределение удельных биомасс доминантов растительности у северо-западного берега Японского моря по широте. По оси абсцисс – широта (градусы), по оси ординат – удельные биомассы (кг/м2). Показаны линии регрессии (красные линии)
Так, на юге района преобладает Saccharina japonica с удельной биомассой до 15–24 кг/м2, которая определяет общий облик растительности. Однако на участке 50º с.ш., у мыса Сюркум, облик растительности меняется: севернее мыса S. japonica исчезает. Здесь проходит северная граница ареала этого вида. Картину дополняет исчезновение Kjellmaniella crassifolia и Corallina pilulifera. Они замещаются видами, удельные биомассы которых возрастают к северу от мыса Сюркум: S. cichorioides (от 0,41±0,12 до 2,74±0,96 кг/м2 при р=0,03), Costaria costata (от 0,21±0,10 до 2,05±0,37 кг/м2 при p=0,04) и Agarum clathratum (от 1,10±0,17 до 1,88±0,50 кг/м2 при p=0,04). Широтные изменения растительности района статистически значимы (см. табл. 3). Формирование дискретной фитоценотической границы у 50º с.ш. связано с наличием географического препятствия – мыса Сюркум (Лоция, 2003). Градиенты обилия образуют континуальные элементы структуры растительности и соответствуют местным особенностям: постепенному уменьшению ширины пояса твердых грунтов с юга на север, обусловленному снижением гидродинамической нагрузки по мере сужения Татарского пролива к северу.
Таблица 3. Характеристики широтных градиентов растительности у северо-западного берега Японского моря Table 3. Characteristics of latitudinal vegetation gradients along the northwestern coast
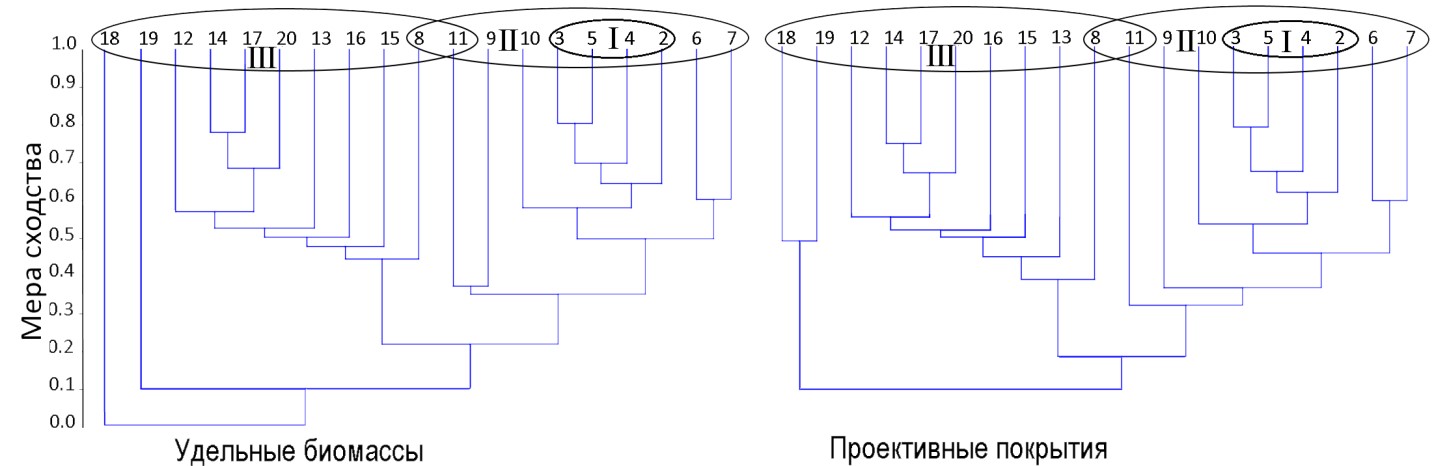
Что касается вертикального распределения доминантов, 2/3 из них наиболее часто встречаются на глубинах менее 6 м. Для 13 (почти 2/3 видов) не выявлено статистического значимого снижения удельных биомасс с глубиной, а для четырех видов (Ulva fenestrata, Agarum clathratum, Odonthalia corymbifera, Zostera asiatica) удельные биомассы, независимо от глубины, остаются на одном уровне. Эти обстоятельства характеризуют меру устойчивости показателей обилия адаптивной зоны пояса растительности под воздействием глубинного градиента. Статистически значимое снижение удельных биомасс с глубиной отмечено только для 8 проанализированных доминантов (табл. 3). Дендрограммы сходства растительности по глубине, построенные по удельным биомассам и проективным покрытиям, оказались близки между собой (рис. 9). Выделяется по 2 больших группы кластеров, охватывающих частично перекрывающиеся диапазоны глубин 2–11 и 8–20 м и группы, включающие глубины 2–5 м. Они показывают расхождение общей адаптивной зоны пояса растительности на более узкие зоны, приуроченные к своим глубинам. Картина имеет признаки континуума. В горизонте растительности выделяется 3 этажа. Их расположение соответствует предложенной ранее стратификации (Дуленин, 2008), однако вместо дискретных границ они имеют широкие переходные зоны: на глубинах 5–6 м и 8–11 м и 18–22 м. Ниже, до глубин 40–42 м располагается горизонт разреженных поселений вне пределов адаптивной зоны растительности.
Рис. 9. Сходство состава и обилия доминантов подводной растительности северо-западного берега Японского моря по глубине. Арабскими цифрами показаны глубины в метрах, римскими – номера этажей верхнего горизонта сублиторали, овалами – границы этажей
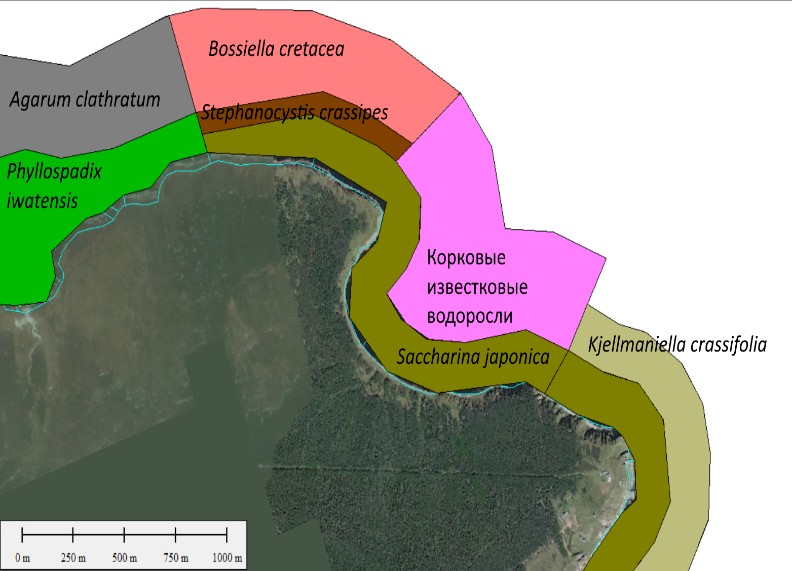
На ландшафтном инфраценотическом уровне выражена поясная структура растительности: выделяется до 5 ценотических поясов, при этом на отдельных разрезах их количество всегда меньше. Вдоль наиболее типичных для района абразионных берегов, ниже клифа, на пологой валунной отмостке бенча с глубинами от 0 до 5–6 м располагаются по 1 или 2 пояса растительности. У самого берега формируются пояса филлоспадикса иватенского, перемежающиеся с поясами сахарины японской, которая к северу от ценотической границы у мыса Сюркум замещается сахариной цикориевидной. На границе склона и валунной отмостки сахарины сменяются поясами представителей сем. Sargassaceae, а еще ниже – поясами агарума продырявленного. На максимальных глубинах пояса образуют членистые и корковые известковые водоросли – представители порядка Corallinales (рис. 10). Количество ценотических поясов на каждом разрезе, против ожидания, довольно мало – 1,9±0,07(1–4) и статистически значимо уменьшается с юга на север (α=-0,13±0,06, R2=0,004, p=0,03). Однако общее количество разрезов, на которых обнаружено более одного пояса, почти двукратно превышает количество разрезов с единственным ценотическим поясом – 88 против 47 разрезов соответственно. Общая конфигурация пояса растительности существенно меняется в широтном направлении: его глубина распространения (14,5±0,5(6–22) м, α=–1,9±0,3, R2=–0,2, p<0,0001) и ширина (495±50(25–3000) м, α=–0,13±0,06, R2=0,04, p=0,03) уменьшаются к северу вслед за шириной пояса абразионных бенчей и денудационных склонов. В целом район характеризуется сочетанием дискретных и континуальных элементов сложения растительности.
Рис. 10. Смена ценотических поясов с доминированием отдельных видов на одном из участков северо-западного берега Японского моря
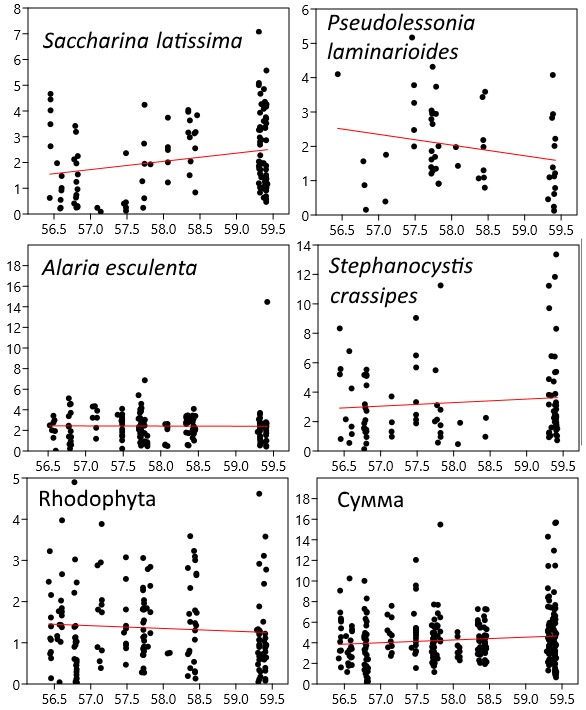
У северо-западного берега Охотского моря на региональном инфраценотическом уровне, в отличие от южного модельного района, выделяются лишь 5 доминантов (рис. 11, табл. 4). Их состав неизменен по всему району. Исключение составляет Zostera marina, обитающая в единственном рефугиуме – мелководном и относительно хорошо прогреваемом заливе Алдома. В Охотском море помимо пространственных характеристик растительности получены данные о ее временнóй изменчивости. Показатели обилия большинства доминантов (Alaria esculenta, α=0,09±0,009, R2=0,23, p<0,0001; Stephanocystis crassipes, α=0,06±0,02, R2=0,07, p=0,002; Rhodophyta, α=0,04±0,006, R2=0,02, p<0,0001) и пояса растительности (α=0,09±0,01, R2=0,02, p<0,0001) статистически значимо растут с течением времени, вероятно вследствие потепления и уменьшения ледовитости моря (Зуенко и др., 2019). Изменения структуры растительности наблюдаются только на границах района и обусловлены географическим препятствием (полуостровом Лисянского) на северо-востоке и изменением геоморфологической структуры берегов на юго-западе. Широтные изменения обилия доминантов (кроме Saccharina latissima, табл. 4) статистически незначимы.
Рис. 11. Распределение удельных биомасс доминантных видов растительности северо-западного берега Охотского моря в широтном направлении. По оси абсцисс – широта (градусы);
Пояс растительности района приурочен к мелководьям: 78% проб собрано на глубинах до 6 м. В отличие от выраженной стратифицированности растительности ряда других районов Дальнего Востока (Гусарова, 1975; Перестенко, 1980; Бывалина и др., 1985, и др.), здесь одни и те же доминанты произрастают от верхних до нижних границ растительного покрова. Ни для одного доминанта не отмечено статистически значимого снижения обилия с глубиной (табл. 4). Суммарные удельные биомассы имеют выраженный глубинный градиент только благодаря преимущественной приуроченности к мелководьям одного из доминантов – Pseudolessonia laminarioides. Таким образом, в отличие от Японского моря, растительность северного модельного района на региональном инфраценотическом уровне относительно однородна и характеризуется выраженными континуальными чертами сложения. Вдоль трехсоткилометрового участка на северо-востоке района, у преобладающих на этом участке аккумулятивных берегов, подводной растительности нет из-за отсутствия подходящих твердых грунтов для прикрепления водорослей-макрофитов. Однако вдоль большей части побережья, на протяжении около 600 км, растительность хорошо развита вдоль преобладающих денудационных берегов.
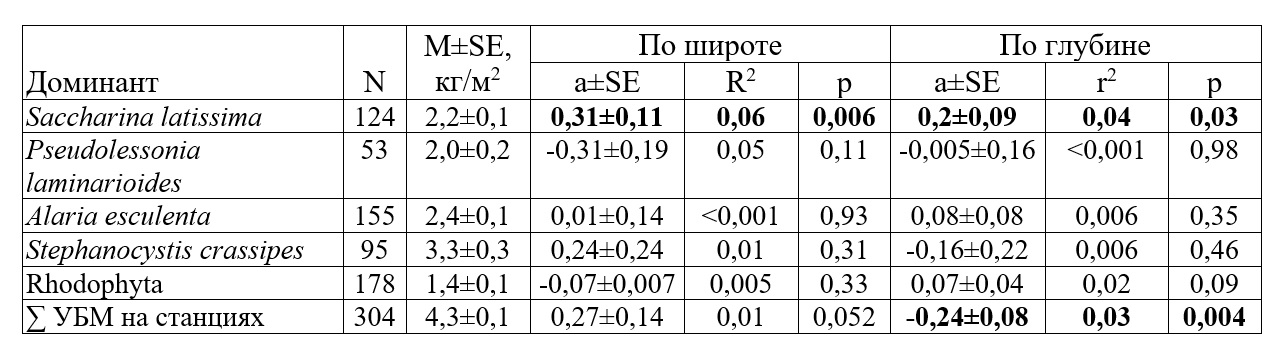
Таблица 4. Характеристики градиентов растительности северо-западного берега Охотского моря на региональном инфраценотическом уровне по данным 2020 г. Table 4. Characteristics of vegetation gradients off the northwestern Sea of Okhotsk coast at the regional infracoenotic level according to 2020 data
Общая конфигурация пояса растительности сильно отличается от южного модельного района. Глубины ее распространения составляют лишь 5,4±0,2(2–11) м, т.е. в 2,7 раза меньше япономорской, а ширина пояса 270±24(50–1000) м, т.е. в 1,8 раза меньше, чем в Японском море. Обе величины не имеют значимых широтных трендов (глубина распространения – α=0,3±0,2, R2=0,03, p<0,07, а ширина – α=15±28, R2=0,002, p<0,59). На ландшафтном уровне растительность также отличается от япономорской. Среднее количество ценотических поясов равно 1,5±0,07. Суммарное количество разрезов с выраженной поясностью почти двукратно меньше ценотически однородных разрезов (45 и 81, соответственно). Характер смены адаптивных зон на неоднородных участках пояса растительности показывает, что это не последовательная смена ценотических поясов с глубиной, как в Японском море, а однородные профили растительности либо хаотичное расположение различных адаптивных зон на разных глубинах. Итак, имеющиеся материалы позволили дать количественную характеристику общих адаптивных зон растительности модельных районов и статистически показать степень их неоднородности. В южном районе сублиторальная растительность относительно богата и разнообразна. На инфраценотическом уровне она сочетает в себе дискретные и континуальные элементы. Северный модельный район отличается относительно бедной и однородной растительностью с выраженными континуальными чертами. В соответствии с гипотезой 1, высказанной во Введении, количественные градиенты пояса растительности оказались выражены в южном модельном районе и не выражены либо слабо выражены в северном. Общие характеристики растительности модельных районов обусловлены местными географическими и геоморфологическими особенностями, что подтверждает гипотезу 2. У выровненных аккумуляционных берегов, в полном соответствии с гипотезой 3, растительный пояс отсутствует. Растительность районов соответствует симпсоновской модели сложных адаптивных зон, внутри которых выделяются пояса и мозаики подчиненных адаптивных зон отдельных видов. Их было целесообразно описать в качестве ассоциаций сублиторальной растительности. Ассоциации сублиторальной растительности модельных районов. Результаты описания растительных ассоциаций модельных районов опубликованы ранее (Дуленин, 2023, 2024б). Здесь дан пример описания ассоциации Stephanocystetum crassipae Dulenin 2024. Это единственная из ассоциаций макроводорослей, общая для обоих модельных районов, что делает интересным сравнение характеристик ассоциации в их пределах. Ее номенклатурный тип (holotypus hoc loco) приведен в табл. 5, облик и распространение – на рис. 12, характеристики модельных районах – в табл. 6 и 7.
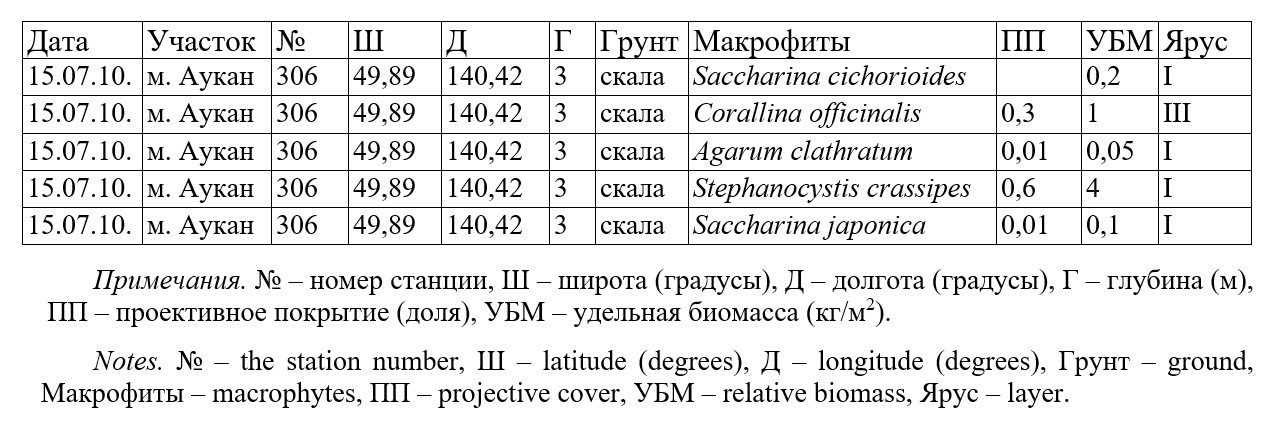
Таблица 5. Номенклатурный тип асс. Stephanocystetum crassipae. Фрагмент электронной таблицы с первичным описанием Table 5. Nomenclatural type of the assotiation Stephanocystetum crassipae. Fragment of an electronic table with the primary description
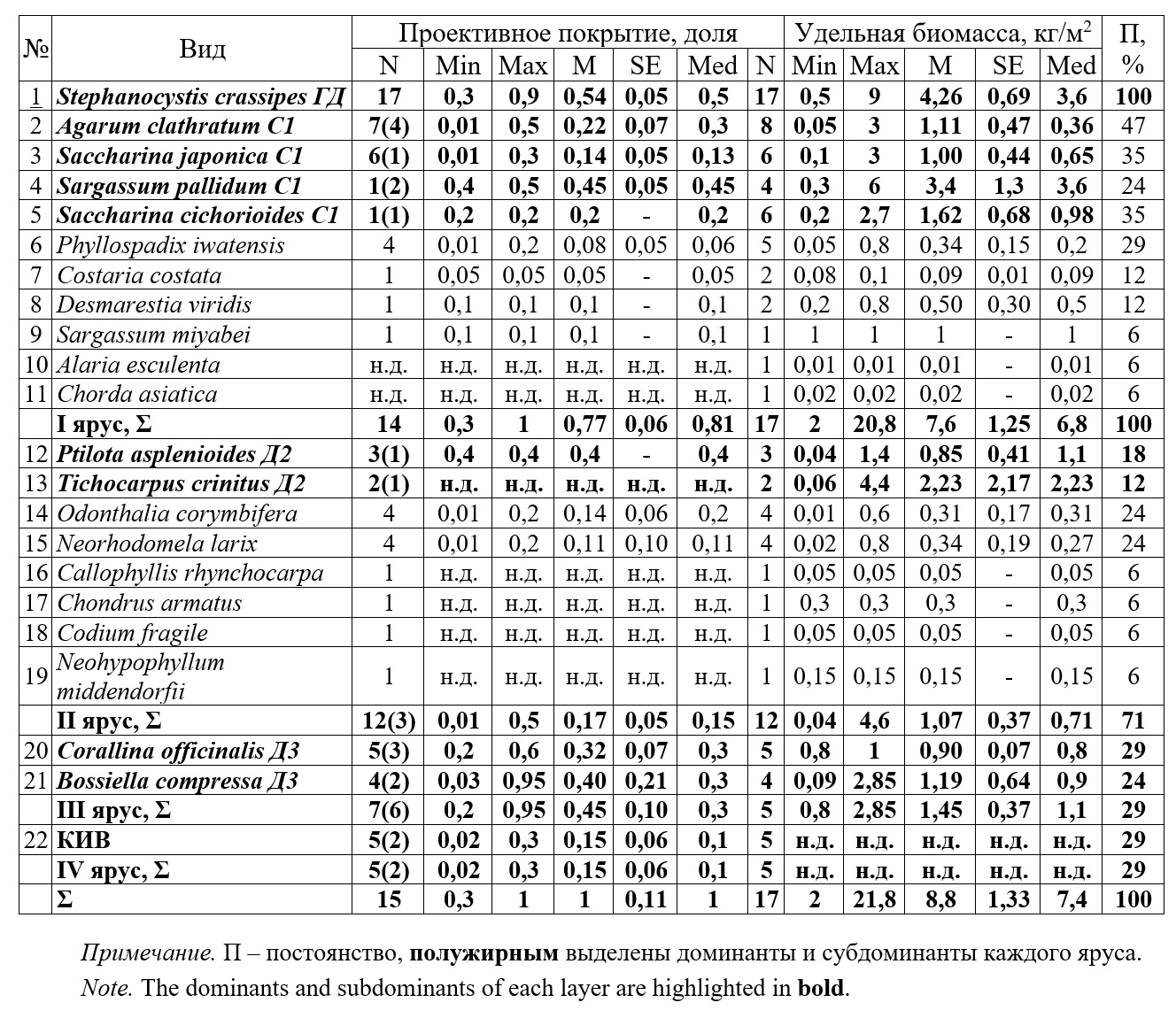
Таблица 6. Качественные и количественные характеристики ассоциации Table 6. Qualitative and quantitative characteristics of the Stephanocystetum crassipae association off the Sea of Japan northwestern coast
Диагностический вид – Stephanocystis crassipes. Ассоциация региональная, распространена повсеместно в обоих модельных районах как у открытых побережий, так и в полузащищенных местообитаниях. Образует фитоценозы на скалистых, глыбовых, валунных и галечных грунтах при уклоне от незаметного до слабонаклонного. Формируется на глубинах от 2 до 10 м. Высота растительного покрова до 3 м. Образована преимущественно многолетними растениями. Формирует легко доступные для промыслового освоения поселения. В Японском море глубины ее распространения статистически значимо уменьшаются к северу (α=-0,52±0,16, R2=0,1, p=0,002). Выявленная частота встречаемости – 3%. В ассоциации выражено до 4 ярусов. Ее ценофлора насчитывает не менее 22 видов, однако в отдельных описаниях отмечено лишь от 1 до 8, в среднем – 4 вида. Монодоминантны 40% фитоценозов. В северном модельном районе характеристики ассоциации сильно отличаются от южного. С юга на север ассоциации распределяется по глубине статистически равномерно (α=0,06±0,08, R2=0,04, p=0,46). В ценофлоре отмечено 6 видов (табл. 7) против как минимум 22 видов в Японском море. В сборах отмечали от 1 до 4, в среднем 1,6 вида. В качестве субдоминантов отмечены 3 вида в I ярусе, в качестве доминантов II яруса – красные водоросли.
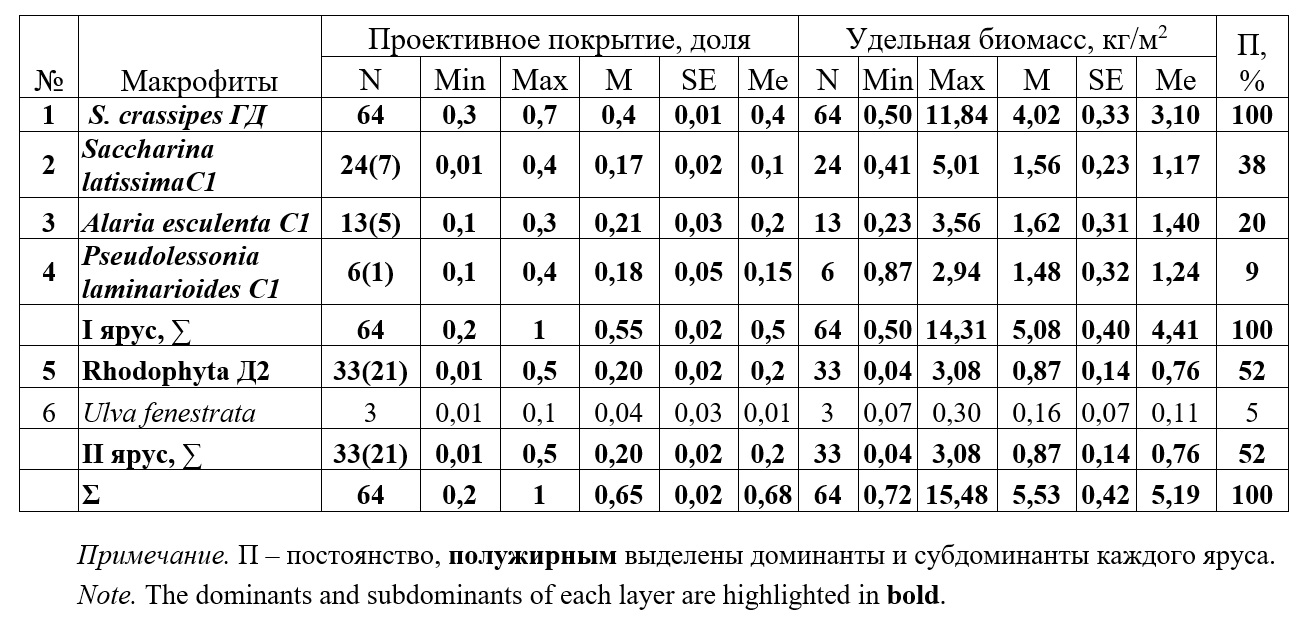
Таблица 7. Качественные и количественные характеристики ассоциации Stephanocystetum crassipae у северо-западного берега Охотского моря Table 7. Qualitative and quantitative characteristics of the Stephanocystetum crassipae association off the Sea of Okhotsk northwestern coast
Экотопические условия формирования ассоциации сходны с таковыми для Японского моря. Однако выявленная частота встречаемости ассоциации в обсуждаемом районе – 21% против 3% в Японском море (Дуленин, 2021). Таким образом, в Охотском море ассоциация стефаноцистиса весьма широко распространена, формируя пятую часть растительного покрова дна. Среднее суммарное проективное покрытие в ассоциации 0,65 и средняя удельная биомасса 5,53 кг/м2 против 1 и 8,8 кг/м2 в Японском море, соответственно. Монодоминантными были 14% фитоценозов ассоциации против 40% в обследованной части Японского моря. Таким образом, макрофиты ассоциаций стефаноцистиса в различных районах реализуют существенно различающиеся жизненные стратегии. В Охотском море фитоценозы ассоциации захватывают большие площади дна, имея относительно низкие показатели обилия, тогда как в условиях высокой конкуренции за субстрат на мелководьях Японского моря (Дуленин, 2021) они достигают значительных показателей обилия на небольших площадях. Индекс доминирования Броцкой–Зенкевича, рассчитанный для ассоциации в Охотском море, составил 1,08, тогда как в Японском – 0,51. Это позволяет говорить, что в борьбе за существование главный доминант ассоциации почти в 2 раза более успешен в северном модельном районе по сравнению с южным. Всего в южном модельном районе описано 16 ассоциаций и одна группа фитоценозов (Дуленин, 2021). В северном модельном районе описано 5 ассоциаций и одна группа сообществ (Дуленин, 2023), т.е. его ценотическое богатство в 3 раза ниже, чем в южном районе. Ценофлоры южного района также в 3 раза богаче северного: 18,7±1,8(7–31) видов против 5,6±0,2(5–6) видов. Максимальное богатство япономорских ценофлор в 6 раз больше охотоморских. Видовое богатство ценофлор южного модельного района выявлено на относительно небольшом количестве описаний: 16,2±3,9(3–55). В северном районе ассоциации выделены по 60,4±12(20–90) описаниям. Показано, что богатство ценофлоры ассоциации зависит от количества описаний и имеет вид кривой Берталанфи с относительно узкими доверительными границами. Если описаний не менее 20, количество видов ценофлоры стабилизируется и почти не увеличивается по мере роста количества описаний, приближаясь к асимптотическому значению. Эта закономерность является частным случаем зависимости «виды–площадь» (Кафанов, Жуков, 1993). Из графиков следует, что ценофлоры ассоциаций, выделенных не менее, чем по 20 описаниям, изучены достаточно полно, а их списочный состав близок к действительному, что позволяет использовать имеющиеся данные для анализа структуры ассоциаций (Дуленин, 2024а). Постоянство встречаемости видов ценофлор не превышает 50%, т.е. они лишены явно выраженной связи с синтаксонами. Иными словами, «верные» виды (Миркин и др., 1989) отсутствуют, а диагностировать сообщества по их сочетаниям невозможно. Из сказанного следует, что избранная модель элементарного петерсеновского сообщества, где единственный главный доминант определяет структуру этого сообщества, наиболее адекватна для описания растительности модельных районов, а собственно флористический подход для классификации их растительности бесперспективен. Показатели обилия каждой ассоциации создаются преимущественно за счет ее главного доминанта. В южном модельном районе главные доминанты ассоциаций формируют в среднем 58% проективного покрытия и 53% удельной биомассы, а в северном – 75% и 74% соответственно. У япономорских берегов уровень сходства ценофлор ассоциаций, выделенных не менее, чем по 20 описаниям, весьма высок – от 82 до 98%. В их составе обнаружено 39 видов, т.е. 91% видов, для которых удалось собрать количественные данные. Иными словами, все проанализированные ассоциации включают в состав своих ценофлор подавляющую часть массовых видов, а находки всех видов, кроме главного доминанта, в каждой ассоциации случайны. В северном модельном районе ценофлоры ассоциаций водорослей сходны на 100%. Таким образом доказано, что рассмотренные ассоциации являются элементарными петерсеновскими сообществами (Дуленин, 2024а). Независимо от районов и используемых показателей наблюдается кратное снижение обилия главных доминантов вне пределов своих ассоциаций – в среднем в 2,8 раза по проективному покрытию и в 4,2 раза по удельной биомассе в южном модельном районе и в 2,2 раза по обоим показателям в северном. Различия обилия главных доминантов в своих ассоциациях и вне их пределов статистически значимы (p≤0,001, тест Колмогорова-Смирнова). Следовательно, такое снижение обилия закономерно, а утверждение о том, что ассоциации формируются в пределах адаптивных зон своих главных доминантов, не поддается статистическому опровержению. Механизмы захвата субстрата покровообразующими видами уже обсуждались (Miller et al., 2018; Layton et al., 2019; Shelamov et al., 2022). Вероятно, они универсальны и обеспечивают формирование адаптивных зон в районах с выраженным доминированием видов. Адекватность модели ассоциации, как мозаики элементарных петерсеновских сообществ в пределах адаптивных зон, подтверждается данными об относительной площади, занятой фитоценозами ассоциаций модельных районов. В Охотском море описанные ассоциации занимают 88% площади дна (Дуленин, 2023). Лишь оставшиеся 12% приходятся на разреженные поселения. В Японском море эта доля ниже – 68% (Дуленин, 2021) за счет большей относительной площади экотонов, существующих между более разнообразными сообществами. Сказанное позволяет рассматривать сообщества макрофитов с точки зрения петерсеновского подхода, как статистический ансамбль видов (Несис, 1977). Описанная картина отвечает концепции адаптивной зоны (Волвенко, 2018). Это значит, что для опознания ассоциации необходимо и достаточно выделить главный доминант описываемого участка. Визуально хорошо опознаются 65% ассоциаций южного и 83% ассоциаций северного модельных районов (Дуленин, 2024б). Для идентификации остальных необходим отбор проб со дна. Участки расположения фитоценозов соответствуют участкам расположения адаптивных зон главного доминанта каждой ассоциации. Из этого следует, что обозначенную во введении проблему согласования описаний сообществ, выполненных разными авторами, и состоящую в выделении произвольного количества доминантов и субдоминантов, легко решить на основании концепции адаптивной зоны и модели элементарного петерсеновского сообщества. В этом случае необходимо сравнивать не весь флористический и доминантный состав сообществ, а только их главные доминанты. Сравнение сублиторальной растительности районов Дальнего Востока России. Анализ литературных данных и сведения о структуре растительных сообществ двух модельных районов позволили применить концепцию адаптивной зоны для инвентаризации и сравнения сублиторальной растительности дальневосточных морей России в целом. Для этого использованы приведенные в литературе количественные данные либо словесные указания на то, что для отдельных видов формируются свои адаптивные зоны, т.е. каждый вид количественно преобладает над всеми другими на некотором множестве участков. Эти адаптивные зоны описаны в качестве растительных ассоциаций. В сублиторали морей Дальнего Востока России по собственным и литературным данным выделено 67 ассоциаций. Их списки сведены в аналитические таблицы, показывающие их по районам и ярусам растительности. Здесь (табл. 8) для примера приведена таблица распределения ассоциаций бурых водорослей (Phaeophyceae Kjellman 1891), формирующих основу растительного покрова сублиторали региона.
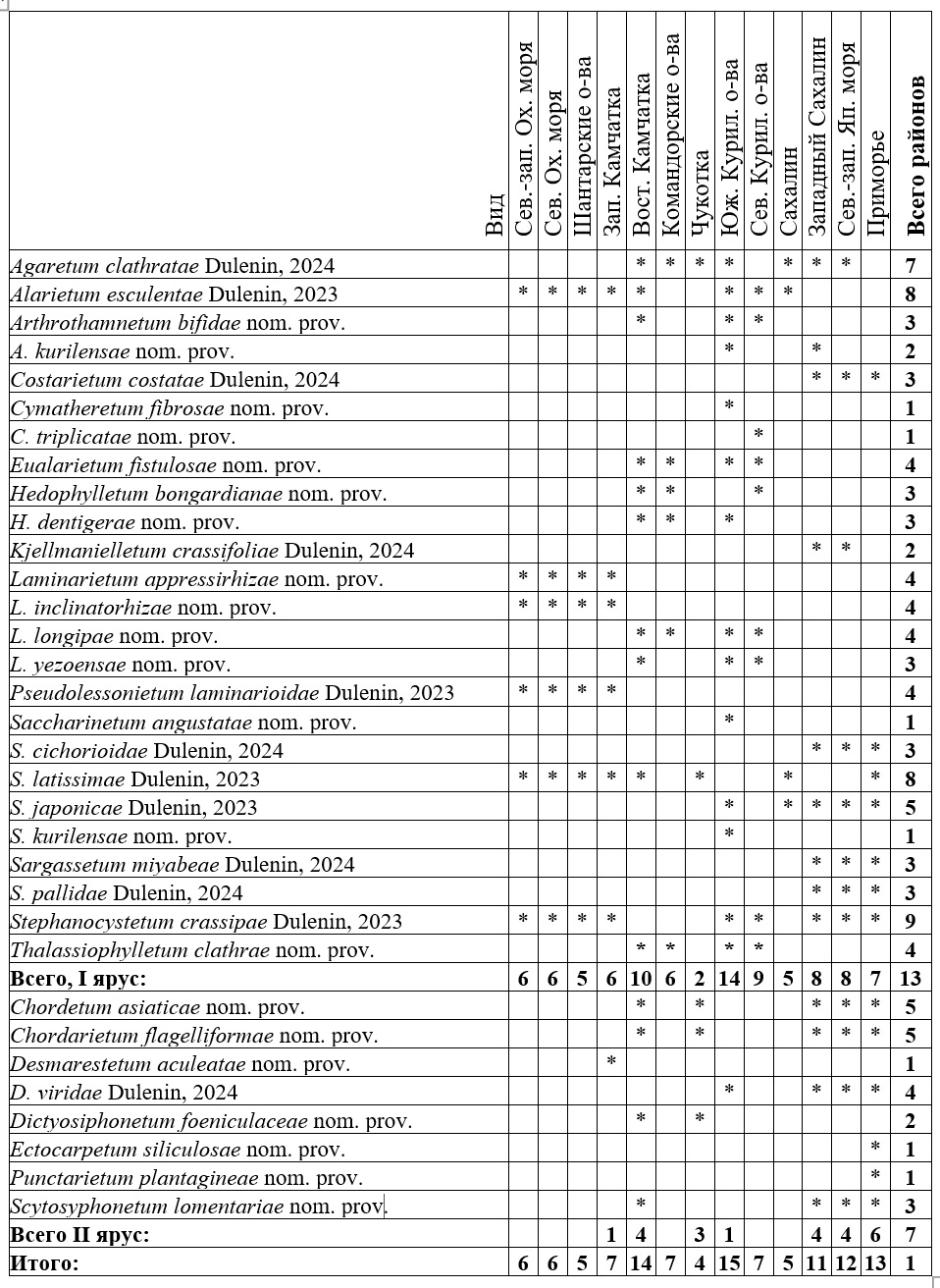
Таблица 8. Распространение ассоциаций бурых водорослей в районах Дальнего Востока России (по: Дуленин, 2024а) Table 8. Distribution of brown algae associations in the regions of the Russian Far East
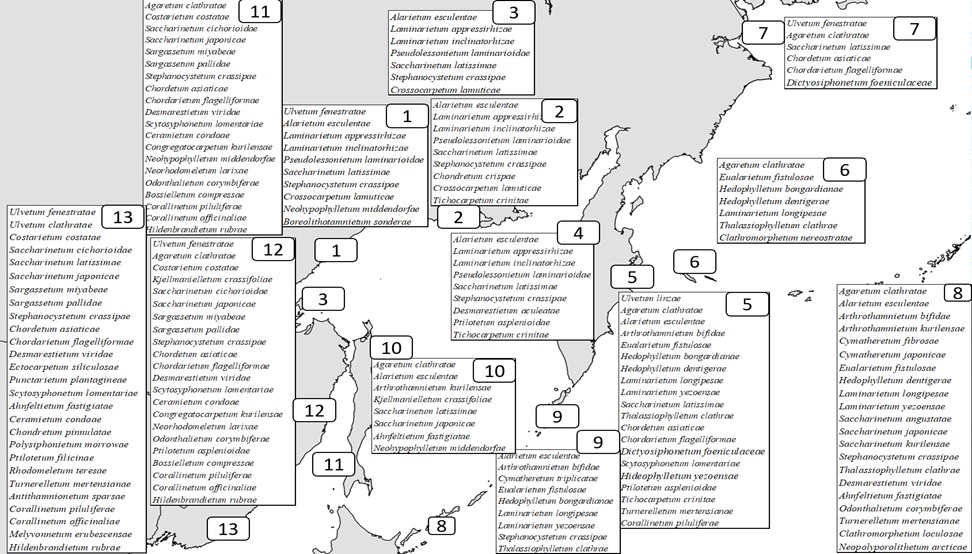
Такие таблицы создают техническую основу для инвентаризации сублиторальной растительности, анализа ее богатства и распространения ее элементов в регионе. Кроме того, они сами по себе представляют информационную ценность, поскольку позволяют визуализировать экосистемные характеристики растительности региона. Анализ пробелов в этих таблицах позволяет предполагать наличие элементарных петерсеновских сообществ ряда доминантов в районах, где они еще не обнаружены и планировать дальнейшие ценологические исследования. Полная картина распределения выделенных растительных ассоциаций по районам Дальнего Востока России приведена на рис. 13.
Рис. 13. Географическое распределение выделенных ассоциаций сублиторальной морской растительности в районах Дальнего Востока России. Цифрами обозначены районы как на рис. 2 (из: Дуленин, 2024а) Рис. 13. Географическое распределение выделенных ассоциаций сублиторальной морской растительности в районах Дальнего Востока России. Цифрами обозначены районы как на рис. 2 (из: Дуленин, 2024а)
Fig 3. Geographical distribution of the identified associations of sublittoral marine vegetation in the areas of the Russian Far East. The numbers indicate the regions as in Fig. 2 (from: Dulenin, 2024а) THE FULL-SIZED IMAGE CAN BE SEEN BY CLICKING ON THE LINK
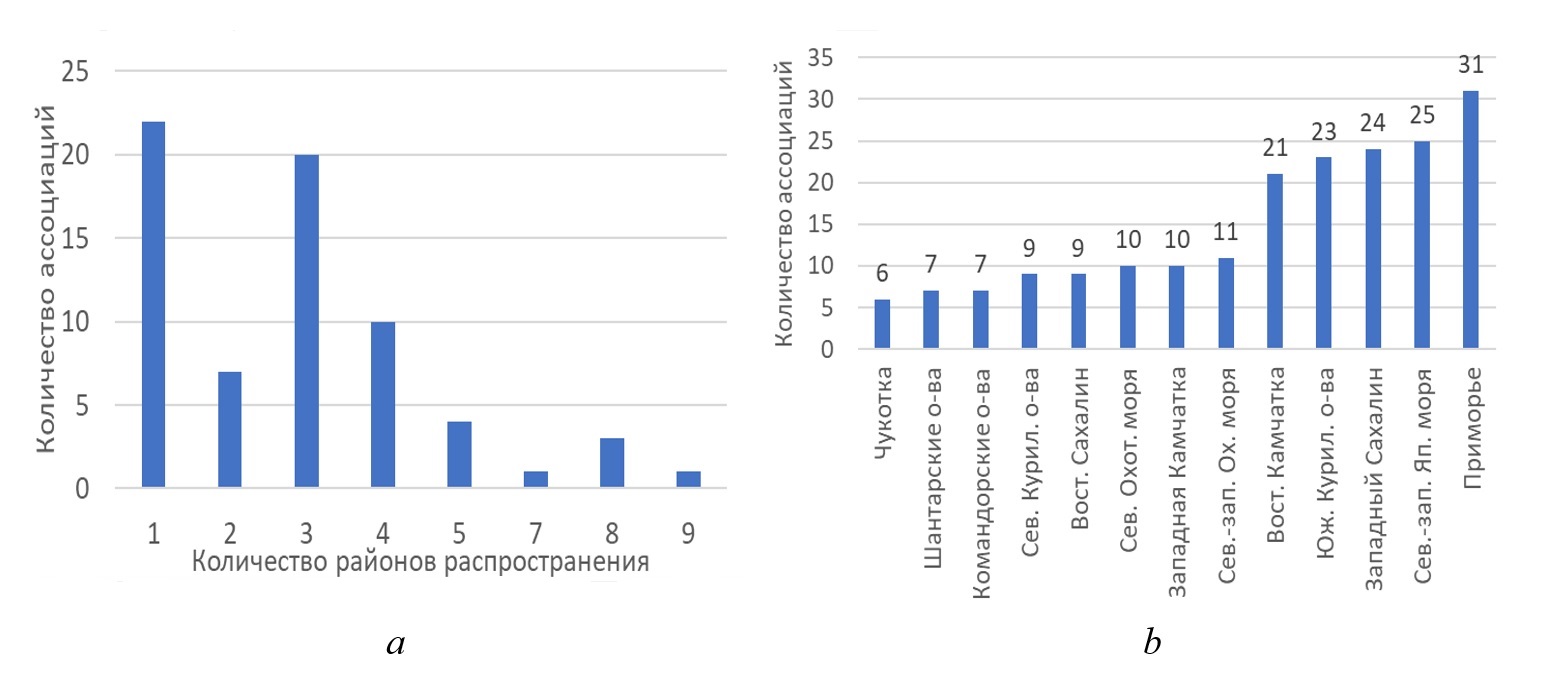
Ассоциации бурых водорослей распространены во всех районах Дальнего Востока, 25 их доминантов формируют I ярус растительности, а 9 – II ярус. Величина относительного ценотического богатства, т.е. доли сообществ отдельного района от количества сообществ всего региона, составляет 8–24%, в среднем 13±2%. График распределения количества ассоциаций по районам (рис. 14 a) имеет трехмодальное распределение, что позволяет выделить 3 группы ассоциаций. Почти третья часть из них распространены узко – в пределах только одного района. Около половины (51%) распространены в 2–5 районах, часто соседних. Наконец 9% максимально широко распространенных сообществ встречаются в 7–9 районах. Их слагают широко распространенные в северном полушарии Земли виды (Agarum clathratum, Alaria esculenta, Zostera marina и т.д.). Умеренно и широко распространенные доминанты составляют основу сублиторальной растительности морей Дальнего Востока. Распределение ассоциаций по районам Дальнего Востока России показано на рис. 13. Ранжирование количества ассоциаций по районам (рис. 14 b) характеризует общее ценотическое богатство районов и позволяет выделить две группы ассоциаций: ценотически бедные 8 районов, в которых обнаружено 5–11 сообществ, и ценотически богатые 5 районов, где найдено от 19 до 32 сообществ.
Самые бедные районы – Чукотка и Шантарские острова, где указано по 6 и 7 ассоциаций соответственно, а самый богатый район – Приморье с 31 ассоциацией. Ценотически бедные регионы как правило самые северные и холодноводные. Западная Камчатка и восточный Сахалин оказались ценотически бедны не только из-за климатических условий, но и благодаря преобладанию у своих берегов аккумулятивных грунтов, не подходящих для прикрепления водорослей в соответствии с гипотезой 3, высказанной во Введении. Уменьшение же ценотического богатства районов к северу подтверждает гипотезу 4. Ценотически богатые районы расположены преимущественно на юге Дальнего Востока. Выявленное закономерное увеличение ценотического богатства к югу выражает фитоценотический аспект известного закона Гумбольдта-Уоллеса (Кафанов, Кудряшов, 2000). Кроме того, ценотическое богатство южных районов обусловлено близостью к центру видообразования макрофитов у берегов Японии (Клочкова, 1996) и наибольшим топическим разнообразием прибрежной зоны Приморья (Лоция …, 1984). Уровни сходства ценотического состава районов по результатам кластерного анализа (Дуленин, 2024а) изменяются закономерно. Максимально (на 90%) сходны списки западного Сахалина и северо-западной части Японского моря, что неудивительно, учитывая сходство природных условий противоположных берегов Татарского пролива. Далее, сходными на 73–83% оказались все районы относительно изолированной холодноводной северной части Охотского моря. Степень сходства грозди сообществ открытых морских районов – восточной Камчатки, Командорских и Курильских остров – ожидаемо оказалась относительно небольшой: 42–51%. Сублиторальная растительность Чукотки оказалась в отдельной ветви. Она имеет наименьшую степень сходства с другими районами, что должно быть связано с весьма суровыми климатическими условиями, удаленностью и со слабой изученностью этого района. Наименьшее ценотическое сходство (17%) расположенных рядом модельных районов обусловлено разделяющим районы опресненным лиманом р. Амур, который формирует дискретную биотическую границу. В то же время районы от восточного Сахалина до восточной Камчатки объединяются в одну большую гроздь, а изменение ценотической структуры их растительности имеет, помимо дискретных, и континуальные черты в соответствии с гипотезой 5, высказанной во Введении. Сведения о флористическом богатстве отдельных районов Дальнего Востока (Клочкова, 1998) позволили статистически описать цено-флористический градиент, т.е. зависимость между количеством видов флоры района и количеством формируемых в районе сообществ (Дуленин, 2024а). Он (α=0,14±0,06) хорошо выражен (R2=0,56) и статистически значим при уровне значимости 0,1 (p=0,05). Существование такой зависимости статистически и экологически оправдано: чем богаче флора района, тем больше видов добьются успеха в борьбе за субстрат и найдут условия для формирования собственных адаптивных зон. Помимо теоретического, график имеет практическое значение. В районе, показанном точкой ниже линии регрессии (Командорские острова), количество сообществ значительно ниже среднего (даже за пределами 95% доверительных границ). Это указывает на их недоизученность и позволяет планировать здесь ценологические исследования. Итак, применение концепции адаптивной зоны дало возможность описать ассоциации сублиторальной растительности всех районов Дальнего Востока России, показав основные «горизонтальные» характеристики их распределения. В частности, концепция позволила установить систематические группы, формирующие основу растительности, дать картину распределения сообществ по районам, охарактеризовать уровни ценотического богатства и сходства районов. Результаты анализа позволили выявить и охарактеризовать увеличение ценотического богатства с севера на юг и его связь с флористическим богатством. Полученные результаты позволили перейти к следующему этапу исследования: построить «вертикальную» иерархическую структуру растительности, т.е. выполнить ее синтаксономическую классификацию и составить ее продромус (Дуленин, 2024а). Продромус дальневосточной сублиторальной растительности. Дж. Симпсон (1948) и И.В. Волвенко (2018) подразумевают формирование адаптивных зон для таксонов и экологических групп любого ранга, что дает собственно экологическое основание для иерархической классификации растительности. В этом случае адаптивная зона высшего таксона будет показывать распространение сообществ соответствующего ему синтаксона. Например, синтаксоны класса растительности Zosteretea будут выделены в границах адаптивных зон представителей семейства Zosteraceae (т.е. преимущественно на рыхлых грунтах мелководий, в условиях умеренной или низкой гидродинамической нагрузки), синтаксоны выделенного класса Phaeophycetea – в границах адаптивных зон бурых водорослей (соответственно, от мелководий до максимальных глубин формирования сублиторальной растительности, на твердых грунтах, в условиях сильной, либо умеренной гидродинамической нагрузки) и т.д. Описания их местообитаний в этом случае будут представлять собой характеристики экологических условий формирования соответствующих адаптивных зон. При такой логике выстраивания иерархической системы растительных сообществ доминантные виды синтаксонов будут их диагностическими видами. Описываемые морские сообщества хорошо классифицируются, их синтаксономия близка к естественной классификации, а объем предлагаемых синтаксонов велик. Поскольку ассоциации рассматриваются как элементарные петерсеновские сообщества (Волвенко, 2018), то каждая из них выделена по главному доминанту группы слагающих ее фитоценозов. Высшие синтаксоны диагностируются, если в качестве главного доминанта фитоценоза обнаруживается любой из диагностических видов подчиненных синтаксонов. Множество диагностических видов высших синтаксонов отражает множество их ассоциаций, поименованных по каждому из этих видов. Применение принципа редукционизма (Миркин, Наумова, 2012) позволяет сделать продромус максимально компактным, а избыточные и неоднозначные классификационные построения исключаются. Такой подход на основе модели элементарного петерсеновского сообщества дает решение имеющейся проблемы идентификации синтаксонов (Разумовский, 2011), обеспечивая уверенное опознание сообществ в природе: даже провизорно выделенные синтаксоны имеют однозначный смысл и объем. Ниже в качестве примере приведен сокращенный фрагмент продромуса с частичным описанием синтаксономии класса Phaeophycetea. Код: PHA Класс: Phaeophycetea nom. prov. Характеристика: Морские сообщества литоральных и сублиторальных макроводорослей класса Phaeophyceae умеренных вод приазиатской части Тихого океана. Диагностические виды: все виды, формирующие элементарные петерсеновские сообщества бурых водорослей. Местообитания: Литораль и сублитораль до глубины 25 м на твердых грунтах при уклоне дна от незаметного до отвесного, преимущественно в условиях сильной и умеренной гидродинамической нагрузки у открытых берегов и во внешних частях бухт и заливов, преимущественно в олигосапробных условиях. Распространение: В регионе – Тихий океан и все моря Дальнего Востока России (Скарлато и др., 1967; Возжинская, Блинова, 1970; Перестенко, 1980, 1997; Толстикова, 1980; Петров, Поздеев, 1992; Клочкова, 1996; Галышева, 2004; Евсеева, 2007; Калита, Скрипцова, 2014; Дуленин, 2021, 2023, 2024б). Сообщества морских бурых макроводорослей распространены от арктических до тропических морей по всему миру (Encyclopedia …, 2023). Примечания: Класс выделен по собственным и литературным данным (см. выше).
Код: PHA-01 Порядок: Phaeophycetalia mesoalgosae nom. prov. Характеристика: Морские сообщества сублиторальных макроводорослей класса Phaeophyceae II яруса растительности умеренных вод приазиатской части Тихого океана. Диагностические виды: Chorda asiatica, Chordaria flagelliformis, Dictyosiphon foeniculaceus, Ectocarpus siliculosus, Punctaria plantaginea, Scytosiphon lomentaria. Местообитания: Cублитораль на глубинах до 16 м, на твердых грунтах. Распространение: Японское, Охотское, Берингово моря, Тихий океан (Скарлато и др., 1967; Возжинская, Блинова, 1970; Перестенко, 1980, 1997; Толстикова, 1980; Петров, Поздеев, 1992; Клочкова, 1996; Галышева, 2004; Евсеева, 2007; Калита, Скрипцова, 2014). Примечания: Порядок выделен по литературным данным (см. выше).
Код: PHA-01A Союз: Chordion nom. prov. Характеристика: Морские сообщества макроводорослей семейства Chordaceae Dumortier 1822 умеренных вод приазиатской части Тихого океана. Диагностические виды: Chorda asiatica Местообитания: Японское море: залив Петра Великого (Перестенко, 1980) и Татарский пролив (Клочкова, 1996), Берингово море (Толстикова, 1980). Учитывая распространение союза на крайнем севере и крайнем юге российского Дальнего Востока, вероятно его распространение также у Курильских островов. Распространение: соответствует таковой у порядка. Примечания: Союз выделен по литературным данным (см. выше).
Код: PHA-01A01 Ассоциация: Chordetum asiaticae nom. prov. Характеристика: Морские сублиторальные сообщества макроводорослей с доминированием Chorda asiatica дальневосточных морей России. Местообитания: Сублитораль, на твердых грунтах, в олигосапробных условиях, при нормальной морской солености. Распространение: Японское, Охотское и Берингово моря. Примечания: Ассоциация выделена по литературным данным (Перестенко, 1980; Толстикова, 1980; Клочкова, 1996; Клочкова и др., 2009а).
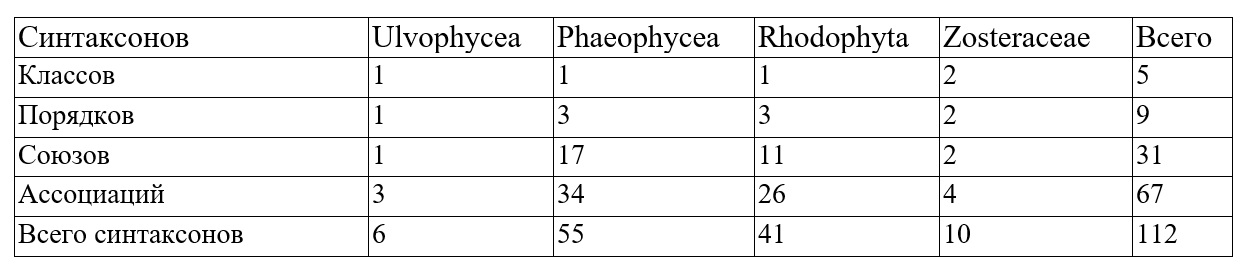
Предложенный продромус содержит характеристики 5 классов, 9 порядков, 31 союза и 67 ассоциаций (табл. 9). Географическое распределение ассоциаций в пределах выделенных районов было показано выше на рис. 13.
Таблица 9. Количество синтаксонов растительности сублиторали дальневосточных морей России (из: Дуленин, 2024а) Table 9. Number of syntaxa of the sublittoral vegetation of the Far Eastern seas of Russia
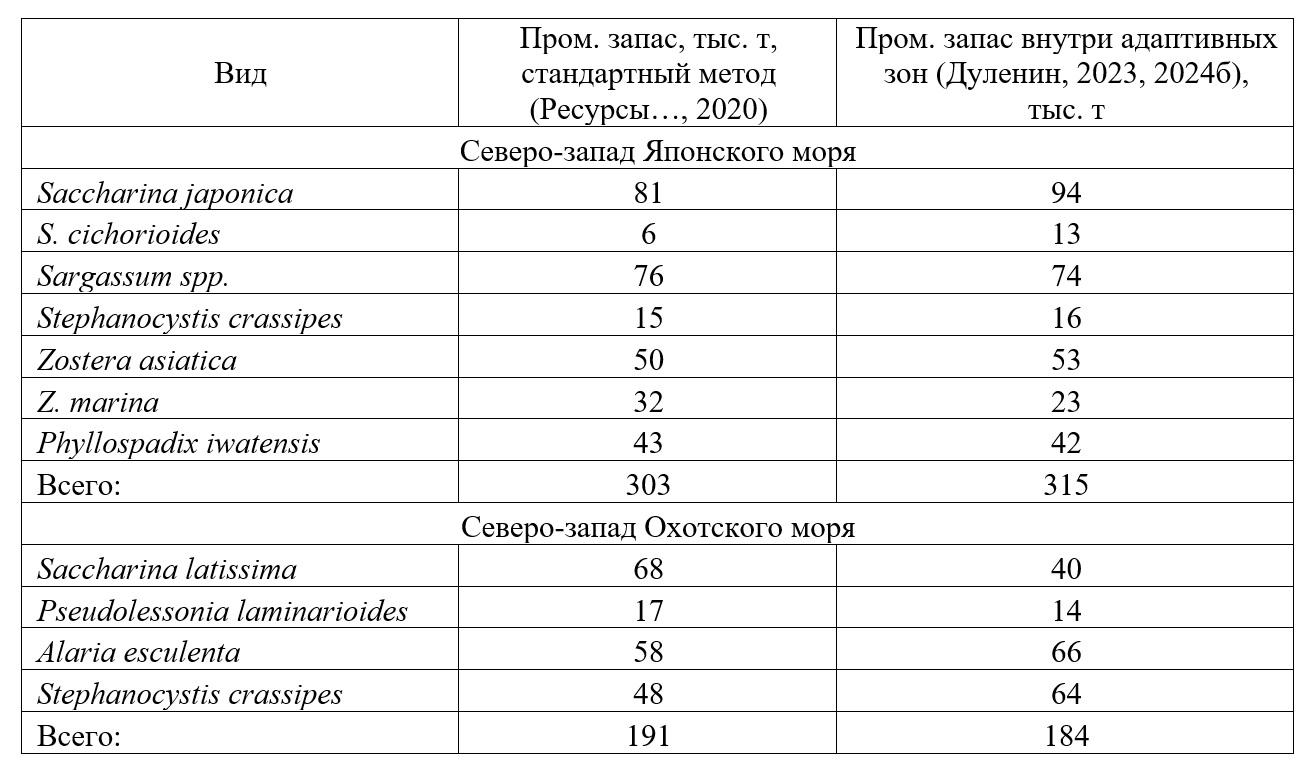
Применение концепции адаптивной зоны к классификации сублиторальной растительности позволило, во-первых, выделить из разнообразных описаний растительности, выполненных разными авторами, виды, формирующие элементарные петерсеновские сообщества, приведя эти описания к «общему знаменателю», и во-вторых, получить сравнимые, воспроизводимые и опознаваемые характеристики донной растительности разных районов, независимо от того, были они выполнены по литературным данным либо по гидроботаническим описаниям. Концепция позволяет однозначно выделять сообщества даже при минимуме данных. Выработанная методика пригодна не только для Дальнего Востока России, но и для всех морских акваторий умеренных и высоких широт при условии выраженного доминирования в них отдельных видов, таксономических или экологических групп растительности, т.е. при условии выявления их адаптивных зон. Некоторые практические следствия применения концепции адаптивной зоны. Концепция адаптивной зоны позволяет решить задачу прямого пересчета характеристик сообществ в величину промыслового запаса, что соответствует общим целям фитоценологических исследований по рациональному управлению растительными ресурсами (Шенников, 1964; Быков, 1978). Площадь, занятая ассоциацией вида, равна площади его промысловых поселений, а биомасса главного доминанта равна его запасу. Величины промысловых запасов макрофитов модельных районов (табл. 10), оцененных общепринятыми методами (Ресурсы …, 2020) и с использованием концепции адаптивной зоны близки и не имеют статистически значимых различий (тест Колмогорова-Смирнова, р=1 для южного и р=0,99 и северного модельных районов). Единственный вид, который осваивается промыслом в модельных районах, – Saccharina japonica (300–500 т ежегодно).
Таблица 10. Сравнение объема ресурсов модельных районов, оцененных разными методами Table 10. Comparison of the resources volume in model areas estimated by different methods
Практический смысл описания сообществ донной морской растительности на основании концепции адаптивной зоны состоит в том, что эти описания могут быть напрямую использованы для оценки площади поселений и объема ресурсов макрофитов. Это придает ресурсным исследованиям естественный экологический смысл. Наращиванию объемов добычи макрофитов препятствует отсутствие дешевых и высокопроизводительных орудий, обеспечивающих селективный промысел. На Дальнем Востоке России перспективно использование салазочных гребенок. Использование гребенок запрещено[1]. Однако в 2000-х годах опыт работы одного из предприятий показал, что салазочная гребенка в сочетании с эхолокацией обеспечивает селективное изъятие главного доминанта – сахарины японской – в пределах адаптивной зоны этого вида и стабильное восстановление его количественных показателей на следующий год. Целесообразно включение гребенок с описанными в работе характеристиками в список разрешенных орудий промысла (Дуленин, 2017).
[1] Приказ № 285 от 06 мая 2022 г. «Об утверждении правил рыболовства для Дальневосточного рыбохозяйственного бассейна // М.: Минсельхоз РФ, 2022. П. 32.15. С. 37.
В северном модельном районе участки растительности служат естественными нерестилищами тихоокеанской сельди Clupea pallasii Cuvier et Valenciennes, 1847 (Тюрнин, 1967; Пономарев, 2012), образуя с нею консортивную связь. После нереста сельди 77% биомассы водорослевого пояса приходится на отложенную икру. Таким образом, внутри пояса макрофитов формируется сезонная адаптивная зона второго порядка, которая является важнейшим элементом структуры общей адаптивной зоны пояса растительности. Количественные и пространственные закономерности распределения обыкрения повторяют общие закономерности распределения пояса макрофитов района (Дуленин, Диденко, 2021). Характеристики этой связи использованы для рационализации учетных работ на нерестилищах сельди (Дуленин и др., 2023). В северных районах Охотского моря имеются возможности развития промысла водорослей с отложенной на них икрой сельди, востребованных на внешнем и российском рынке. Однако в соответствии с правилами рыболовства (Правила …, 2022)[2], запрещается добыча «водорослей и морских трав, на которые отложена икра сельди – повсеместно». Запрет был введен в годы депрессивного состояния охотской сельди (Тюрнин, 1980) для обеспечения ее воспроизводства. В настоящее же время запасы сельди находятся на исторически максимальном уровне (Дуленин, Диденко, 2021; Панфилов, Смирнов, 2022). Объемы добычи обыкренных водорослей могли бы составить сотни тонн. Для этого необходимо исключение запрета на добычу обыкренных водорослей из Правил рыболовства (Дуленин, 2016б). [2] Приказ № 285 от 06 мая 2022 г. «Об утверждении правил рыболовства для Дальневосточного рыбохозяйственного бассейна // М.: Минсельхоз РФ, 2022. П. 2.6. С. 110.
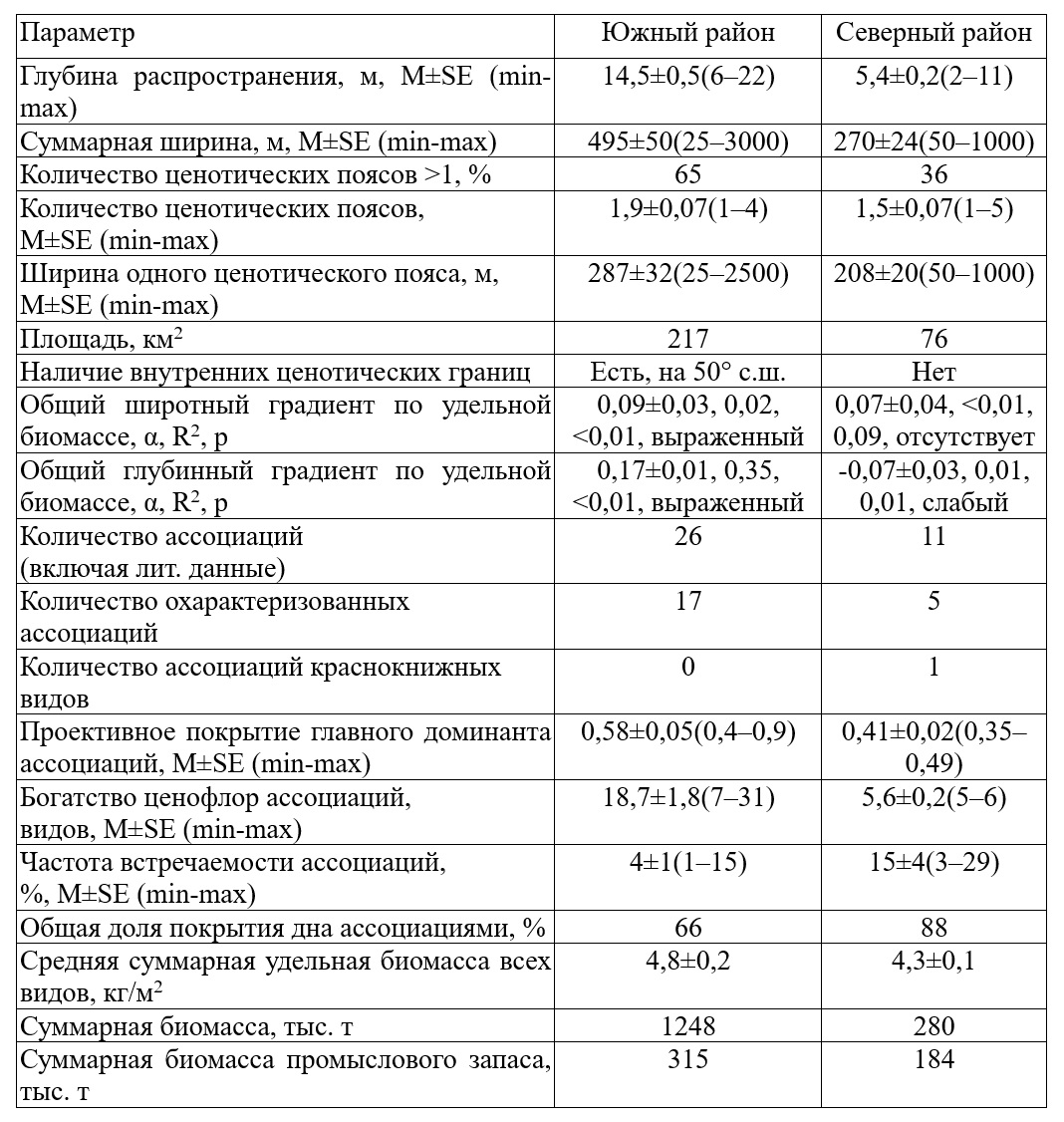
Основным фактором, сдерживающим развитие промысла дикорастущих макрофитов, является их искусственное выращивание. По состоянию на 2022 г., общий объем аквакультуры водорослей в мире составил около 35 млн т, из них в материковом Китае – около 21 млн т (Состояние …, 2022). Между тем, в XIX в. и вплоть до 30-х годов XX в. добываемую на Дальнем Востоке морскую капусту вывозили в Китай (Зинова, 1940; Жариков, 2001). В настоящее время хорошо известен высокий спрос китайских потребителей на пищевые продукты из натуральных, «диких» водных биологических ресурсов. В связи с этим, налаживание экспорта водорослевой продукции в КНР представляется одним из наиболее перспективных путей стимулирования добычи макрофитов на Дальнем Востоке России (Дуленин, 2025а). Вычисление общей величины удельного промыслового запаса сложных адаптивных зон модельных районов и типизация побережий позволяет выполнить оценку промысловых ресурсов всего Дальнего Востока. Для южного модельного района удельный промысловый запас равен 0,5 млн т на 1000 км побережья при протяженности южных районов 3,9 тыс. км, а для северного – 0,2 млн т на 1000 км при протяженности северных районов 8 тыс. км. Общий объем ресурсов макрофитов морей Дальнего Востока оценен в 3,6 млн т (с Eualaria fistulosa, не включенной в расчет по удельному промысловому запасу – 15,6 млн т), что несколько выше прежних оценок (Ресурсы …, 2020) и много выше оценок по данным, полученных в текущем столетии (Евсеева и др., 2024). Суммарная оценка возможного вылова – 360 тыс. т (с Eualaria fistulosa – 1,56 млн т). В итоге все полученные в работе результаты позволяют дать комплексные экосистемные характеристики сложных адаптивных зон модельных районов, которые представляют значительную практическую и теоретическую ценность. По отдельности общие параметры сложных адаптивных зон показаны и обсуждены выше. Они обобщены в таблице 11. Большее богатство и разнородность сложной адаптивной зоны южного модельного района по сравнению с северным закономерна и очевидно имеет характер общего правила с некоторыми исключениями: растительность в низкобореальных районах богаче и разнороднее, чем в высокобореальных. Полученные количественные характеристики адаптивных зон применимы для решения прикладных экологических задач, природоохранных мероприятий, организации рациональной эксплуатации макрофитов и планирования гидробиологических исследований (Дуленин, 2024а).
Таблица 11. Общие экосистемные параметры сложных адаптивных зон поясов Table 11. General ecosystem parameters of complex adaptive zones
Заключение Итак, применение концепции адаптивной зоны к изучению растительного покрова сублиторали модельных районов и морей Дальнего Востока России дало ряд важных практических и теоретических результатов, последовательно вытекающих один из другого: а) На основе принципов использованной концепции разработан и апробирован комплекс методик, позволяющих однозначно и независимо от мнения исследователя опознавать и описывать сублиторальные растительные сообщества непосредственно во время гидробиологических исследований. Благодаря применению современных аппаратных и программных средств объективного контроля (телеуправляемых необитаемых подводных и беспилотных летательных аппаратов, геоинформационных систем) они обеспечивают максимальную степень проверяемости, воспроизводимости и документирования результатов. б) На основе первичных гидроботанических описаний, полученных во время гидробиологических съемок, выполнены единообразные сравнимые описания сублиторальных растительных ассоциаций модельных районов: северо-западных побережий Японского и Охотского морей, снабженные максимально полными статистическими характеристиками их структуры, обилия и пространственного распределения. Они пригодны для решения как теоретических (выявление характеристик сообществ макрофитов), так и практических (оценка воздействия на окружающую среду, природоохранные мероприятия, рациональное использование ресурсов) задач. в) Анализ полученных статистических данных выявил основные характеристики структуры сублиторальных ассоциаций растительности модельных районов. Установлено, что они представляют собой элементарные петерсеновские сообщества: наибольшую долю обилия (биомассы или проективного покрытия дна) в них формирует главный доминант, для которого на участке формирования фитоценоза имеются условия адаптивной зоны, а присутствие остальных видов статистически случайно. г) Концепция адаптивной зоны объясняет возникновение доминирования в растительном сообществе: на каждом участке имеется единственный вид, который более других видов приспособлен к комплексу абиотических и биотических условий данного участка и потому захватывает наибольшую долю площади дна и формирует наибольшие биомассы. д) Установлено, что смена адаптивных зон обусловливает видимую картину вертикальных и горизонтальных фитоценотических границ, наличие количественных градиентов в структуре растительности, смену ее ценотически однородных поясов и локальных фитоценозов. е) Решена принципиальная проблема сравнения описаний растительности, выполненных на основании различных методических подходов. Для этого предложено при сопоставлении разнородных количественных или словесных характеристик растительности различных районов, выполненных разными авторами, выявлять в каждом описании единственный вид растительности, преобладающий по показателям обилия. Благодаря этому выработан единый язык сравнения разнообразных описаний, дающий возможность инвентаризации морской растительности любых районов с выраженным доминированием. ж) Составлены инвентаризационные таблицы со списками доминирующих видов сублиторальной растительности, для которых в морях Дальнего Востока России выявлены адаптивные зоны. Таблицы позволили проанализировать общие инфраценотические закономерности распределения растительности по районам, основным систематическим группам и ярусам. з) Построена максимально простая и близкая к естественной система синтаксонов сублиторальной растительности морей Дальнего Востока России, легко опознаваемых в полевых условиях. Она основана на том принципе, что адаптивные зоны формируются не только для видов, но и для высших таксонов либо экологических групп макрофитов. Предложенная система может быть дополнена при проведении дальнейших исследований. и) Составлен продромус растительности дальневосточных морей России. Его можно использовать в качестве полевого инструмента для опознания синтаксонов разного ранга и как основу для дальнейшей инвентаризации дальневосточной морской растительности. Его можно применить и в качестве основы для составления продромусов соседних регионов. к) Концепция адаптивной зоны использована для оценки промысловых запасов макрофитов модельных районов. Ее использование придает понятный экологический и практический смысл процедурам оценки состояния ресурсов: поскольку в пределах адаптивной зоны вид количественно преобладает на участке, это означает формирование удобных для промыслового освоения поселений. Промысловая разведка представляет собой поиск и инвентаризацию адаптивных зон промысловых макрофитов. л) Пояс донной растительности, будучи «экосистемным инженером», сам создает условия экологических оптимумов и адаптивных зон второго порядка для организмов-консортов на различных стадиях их жизненного цикла (в северном модельном районе – для сельди), определяя общие закономерности их распределения. Перечисленные пункты демонстрируют, что использование концепции адаптивной зоны для изучения донной морской растительности показало ее универсальную применимость: от совершенствования методик гидробиологических исследований и оценки ресурсов до инвентаризации растительности по литературным данным. Одинаково результативное применение концепции адаптивной зоны для описания растительности теплоумеренной северо-западной части Японского моря и холодноводной северо-западной части Охотского моря, как и для других дальневосточных морей России, показывает, что выработанные подходы могут быть применены для изучения и инвентаризации донной растительности любых морей с выраженным доминированием донной растительности. Очевидны перспективы этих подходов и для изучения других групп эпибентоса.
Благодарности. Автор глубоко благодарен своему учителю, к.б.н. И.С. Гусаровой, которая привила мне интерес к исследованию морской растительности. Конфликт интересов. Автор является членом Редколлегии журнала "Вопросы современной альгологии". Процесс рецензирования и принятия решения по данной статье был организован независимо от автора.
Список литературы
Статья поступила в редакцию 04.12.2024
Об авторе Дуленин Александр Алексеевич – Dulenin Alexander A. доктор биологических наук dulenin@khabarovsk.vniro.ru Корреспондентский адрес: 680038, Россия, г. Хабаровск, Амурский бульвар, д. 13а, ХабаровскНИРО; тел. (4212)31-54-47.
ССЫЛКА: Дуленин А.А. Структурирование сублиторальной растительности дальневосточных морей России с точки зрения концепции адаптивной зоны // Вопросы современной альгологии. 2024. № 2–3 (35–36). С. 44–83. URL: http://algology.ru/2235 DOI – https://doi.org/10.33624/2311-0147-2024-2-3(35-36)-44-83; EDN – EHJFCV
Уважаемые коллеги! Если Вы хотите получить версию статьи в формате PDF, пожалуйста, напишите в редакцию, и мы ее вам с удовольствием пришлем бесплатно.
Structuring the sublittoral vegetation of the Russian Far Eastern seas from the perspective of the adaptive zone concept Alexander A. Dulenin Khabarovsk Branch of VNIRO – «KhabarovskNIRO» (Khabarovsk, Russia) An ecologically grounded methodology for identification, description, inventorying, and resource assessment of marine sublittoral vegetation communities is proposed. The sublittoral vegetation belt of Russian Far Eastern seas is formed by a system of adaptive zones of varying ranks, each with a single dominant species accompanied by a statistically random set of other species. Vegetation distribution in specific areas is determined by the geography and geomorphology of their coasts. Any descriptions of plant communities are fundamentally comparable provided that the primary dominant species is identified, for which an adaptive zone is formed within the site. Sixty-seven plant associations have been distinguished in the region, most of which can be unambiguously identified visually. The number of associations decreases from southern to northern regions. The nature of their distribution should be described as the cenotic aspect of the Humboldt-Wallace law. The resources of individual species are associated with their adaptive zones, and the area of their commercial beds equals the area of these zones. Far Eastern macrophyte resources are estimated at 3.6 million tons. Key words: vegetation structure; sublittoral; Russian Far Eastern Seas
References
Dulenin Alexander A. ORCID ID – https://orcid.org/0000-0002-3491-6805 Khabarovsk Branch of VNIRO («KhabarovskNIRO»), Khabarovsk, Russia dulenin@khabarovsk.vniro.ru
ARTICLE LINK: Dulenin A.A. Structuring the sublittoral vegetation of the Russian Far Eastern seas from the perspective of the adaptive zone concept. Voprosy sovremennoi algologii (Issues of modern algology). 2024. № 2–3 (35–36). P. 44–83. URL: http://algology.ru/2235 DOI – https://doi.org/10.33624/2311-0147-2024-2-3(35-36)-44-83; EDN – EHJFCV
На ГЛАВНУЮ
К разделу ОБЗОРЫ, СТАТЬИ И КРАТКИЕ СООБЩЕНИЯ
|
|||
|
| ||